Pockmarks (M. Francoise)
Projet de MatéMatéo Francoise, par Adele Giobbini et Audrey Rouchon.
26/01/2024 :
Les pockmarks sont des cratècratères (dédépressions) situésituées sur le fond marin, pouvant atteindre 350m de diamèdiamètre, 35m de profondeur et une densitédensité de 160/km2 (Belfast Bay, Maine). Ils sont forméformés par l’él’échappement de fluides/ gaz naturel biogébiogénique vers la surface, crécréant ainsi des cratècratères.
MatéMatériel :
- cristallisoir (le plus gros)
- bicarbonate de sodium NaHCO3
- acide (citrique ?
ÀÀ commander ?) C6H8O7 - sable (pour
sésédiment effervescent) - sable (+ argile) (pour fond marin)
- eau
Protocole :
Pour un kilogramme de sable effervescent :
- Dans un
rérécipient, onmémélange 100gd’d’acide citrique, 50g de bicarbonate de sodium et 850g de sable.
Pour le sable «« fond marin »»:
Nous allons tester diffédifférentes méméthodes :
- du sable seul (de
diffédifférentesgranulomégranulométries) - du sable fin avec de
l’l’argile (nous testerons plusieurs proportions)
ProblèProblème : si le fond du cristallisoir est tapissétapissé de sable effervescent, le gaz risque de s’és’échapper vers les bords du cristallisoir et ne formera pas de pockmarks. Pour reméremédier àà cela, nous laisserons une bande de sable non effervescent tout autour du sable effervescent, pour contrer cet effet. Nous testerons plusieurs largeurs de bande.
Dans le cristallisoir, mettre 1 cm de sable effervescent (85% de sésédiment, ici, le sable; 10% d’d’acide citrique et 5% de bicarbonate de soude) : en effet, la masse molaire de l’l’acide citrique est de 176,12 g/mol, et celle du bicarbonate de sodium est de 84 g/mol. On a donc presque un facteur de 1 àà 2 (84 / 176,12 = 0,48), donc il faut presque deux fois plus de masse d’d’acide citrique que de bicarbonate de sodium pour respecter les coefficients molaires de la réréaction acido-basique.
- NaHCO3 + R-COOH CO2 + H2O + RCOO
−− + Na+
On observe donc une libélibération de CO2, qui permet de reconstituer la libélibération de gaz, nénécessaire àà la formation des PockMarks.
Puis, mettre 3 cm de sable fin (pour reconstituer le fond marin).
Enfin, recouvrir d’d’eau.
ProblèProblème : pour filmer, toujours àà la mêmême hauteur et au mêmême angle, il nous faut un trétrépied.
02/02/2024 :
Informations :
Giant sea-bed pockmarks: Evidence for gas escape from Belfast Bay, Maine: https://pubs.geoscienceworld.org/gsa/geology/article-abstract/22/1/59/205977/Giant-sea-bed-pockmarks-Evidence-for-gas-escape
https://fr.wikipedia.org/wiki/Pockmark
https://www.sciencedirect.com/topics/earth-and-planetary-sciences/pockmark
A la place du bicarbonate de sodium, nous utilisons du carbonate de potassium (K2CO3). Cela change donc nos calculs car la masse molaire n’n’est pas la mêmême :
Masse molaire du carbonate de potassium : 138 g/mol
Masse molaire de l’l’acide citrique : 176 g/mol
Donc on environ un facteur de 0,8 : nous avons donc mis 1 gramme d’d’acide citrique pour 0,8 gramme de carbonate de potassium pour respecter le coefficient stœchioméstœchiométrique.
- Protocole :
Pour cette premièpremière expéexpérience, nous avons utiliséutilisé :
bébéchers- cristallisoir
- acide citrique
- carbonate de potassium
- eau
minéminérale - spatule
cuillècuillère- microbalance
- papier pH
- aluminium
- sable
PremièPremièrement, nous avons faire une premièpremière expéexpérience pour tester si l’l’effervescent fonctionnait. Nous avons mélangémélangé 8 grammes de carbonate de potassium et 10 grammes d’d’acide citrique. La réréaction a fonctionnéfonctionné 👍(çça féfé dédé bulles). Nous avons vérifiévérifié si tout l’l’acide avait étéété neutraliséneutralisé, grâgrâce au papier pH : affirmatif (pH de 6).
Puis, nous avons testétesté une premièpremière expéexpérience, en mettant une couche de sable effervescent (un volume de mémélange effervescent (acide citrique + carbonate de potassium) pour deux volumes de sable fin sec), puis une couche de sable fin sans mémélange effervescent, que nous avons enfin recouvert d’d’eau :
MéMélange effervescent + sable.
Couche de sable effervescent + grosse couche de sable fin.
Bubulle.
Nous avons pu voir du positif :
- nous avons mis de
l’l’effervescent sur tout le fond du cristallisoir etl’l’air nes’s’est paséchappééchappé sur lescotécotés L’L’airs’s’est bienéchappééchappé et estremontéremontéàà travers lessésédimentsàà la fin del’expél’expérience, nous avonstestétesté le pH :l’l’acide a bienétééténeutraliséneutralisé car le pHéétait de 6. Cela signifie une que le sable, une foisséchéséché, pourraêêtreréutiliséréutilisé pour cetteexpéexpérience.
Nous avons rencontrer certains problèproblèmes :
- comment verser
l’l’eau ? - comment faire pour que
l’l’eau ne soit pas trouble ? SûSûrement trop demémélange effervescent- pas vraiment de formation de pockmarks (certains petits
««cratècratères»»)
RemontéRemontée d’d’une bulle.
Vers la fin de la réréaction effervescente, nous pouvons observer des marques àà la surface du sésédiment.
9/02/2024 :
Le sable que nous avions laissélaissé àà sésécher la semaine dernièdernière est devenu un sable «« kinékinétique »» : les grains éétaient assez cohécohésifs.
Nous avons donc essayéessayé avec ce sable làlà, car un problèproblème que nous avions pu rencontrer avec le sable fin éétait que celui ci s’s’affaissait tout de suite sans laisser de cratècratère visible.
Dans cette deuxièdeuxième expéexpérience, nous avons utiliséutilisé :
bébéchersbébécher avec du scotch (pour verserl’l’eau)- cristallisoir
- acide citrique
- carbonate de potassium
- eau
minéminérale - spatule
cuillècuillère- balance
- papier pH
- sable
kinékinétique (recyclérecyclé de la semaineprécéprécédente)
Cette fois ci, nous avons mis moins d’d’effervescent car nous avions vu la semaine dernièdernière que çça bullait trop. Nous avons mis 5g d’d’acide citrique et 4g de carbonate de potassium.
Nous avons mis du sable kinékinétique, dans l’l’espoir de pallier àà l’l’effet d’d’effondrement.
Pour les problèproblèmes de versement d’d’eau, nous avons essayéessayé de fabriquer un arrosoir avec un bébécher et du scotch.
Update : fail.
Nous avons réessayéréessayé avec des plus gros trous, et c’c’est le prototype que nous avons utiliséutilisé pour l’expél’expérience 2.
Update : le versement éétait trop puissant et àà remaniéremanié le sésédiment: gros fail.
Les rérésultats, autrement, éétaient sensiblement similaires aux expéexpériences de la semaine. L’L’effervescence éétait toujours trop forte et le sable ne gardait toujours pas les cratècratères. 
Pour cette troisiètroisième expéexpérience, cette fois-ci avec du sable «« normal »» (non kinékinétique) qui avait étéété humidifiéhumidifié puis séchéséché, mais qui éétait encore un peu humide ce qui fait qu’qu’il éétait plus dense (on s’s’est dit que les cratècratères allaient peut êêtre êêtre plus visibles, mais surtout c’éc’était plus pratique pour mieux rérépartir le mémélange effervescent).
Nous avons mis encore moins d’d’effervescent : 1g d’d’acide citrique et 0,8g de carbonate de potassium.
Protocole :
bébéchers- cristallisoir
- acide citrique
- carbonate de potassium
- eau
minéminérale - spatule
cuillècuillère- balance
- papier pH
- sable
légèlégèrement humide
Nous avons fait comme précéprécédemment : nous avons mélangémélangé le mémélange effervescent avec du sable pour la partie inféinférieure puis nous avons recouvert d’d’une bonne couche de sable. Nous avons essayéessayé une autre technique pour verser l’l’eau : juste le brébréchet, sans scotch, mais trètrès rapidement. Cela a un peu remaniéremanié les sésédiments supésupérieurs, ils se sont redéposéredéposés ensuite de façfaçon non uniforme : fail.
Comme précéprécédemment, le sable ne tenait pas : les cratècratères ne se formaient pas. La forme que nous pouvons observer est due au versement de l’l’eau. Par contre, la dose d’d’effervescent éétait correcte : un peu de bulles bien comme il faut (peut etre meme pas assez mais mieux vaut parfois). En effet, l’l’eau en surface éétait donc moins trouble et nous voyons mieux ce qu’qu’ils e passait).
Nous avons essayéessayé une autre fois de crécréer un arrosoir : çça ne coulait pas super bien mais bon çça va. Par contre…contre…
CasséCassé.
Nous avons donc abandonnéabandonné l’idél’idée arrosoir pour trouver des alternatives. Nous avons essayéessayé avec une seringue et cela semble fonctionner plutôplutôt bien.
Pour cette quatrièquatrième expéexpérience, nous avons cherchécherché àà trouver une alternative au sable uniquement : nous avons mélangémélangé donc 1/3 d’d’argile (42g) avec 2/3 de sable (84g). Nous avons aussi mis le mémélange effervescent juste au centre.
Nous avons utiliséutilisé :
bébéchers- cristallisoir
- acide citrique
- carbonate de potassium
- eau
minéminérale - spatule
cuillècuillère- balance
- papier pH
- sable
légèlégèrement humide - argile verte (illite)
- seringue
Nous avons comme précéprécédemment mis une couche de sable (ici mélangémélangé àà de l’l’argile) avec du mémélange effervescent, puis une couche de sable- argile.
Cette fois ci, sûsûrement àà cause du fait que nous avions mis l’l’effervescent majoritairement au centre, ce qui a créécréé un maxi cratècratère/ volcan !
Et pouf plus de dinos.
CRATEEEEEEEEERE !!!!!!!!!
L’L’argile permet de garder la forme du cratècratère, et l’l’eau pénèpénètre tout de mêmême. C’C’est peut êêtre un peu trop impressionnant pour un pockmark.
PB :
- il faut changer la dose de notre
mémélange effervescent car pas la bonne masse molaire - Il faut trouver comment recycler le sable-argile
- notre
modèmodèle nerepréreprésente pas super bien laréalitéréalité car enréalitéréalité, les pockmarks sontplutôplutôt desdédépressionsliéliéesààl’l’affaissement dusésédiment (car la glace fond et laisse un trou), et non pas descratècratères. - Il est difficile de mesurer le pH dans notre
dernièdernièreexpéexpérience,l’l’eau de surfaceéétant verte carmélangémélangéeààl’l’illite, le papier pH devient vert (il faudrait attendre plusieurs heure quel’l’argilesésédimente: flemme).
16/02/2024:
Nous avons recalculérecalculé notre ééquation pour le mémélange car nous avons changéchangé de carbonate sans revérevérifier l’él’équation. Nous nous sommes rendu compte que les coefficients stœchioméstœchiométriques avaient changéchangé et qu’qu’il fallait 3 moles de carbonate de potassium pour 2 moles d’d’acide citrique. Il faut donc mettre 0,96g d’d’acide pour 1g de carbonate, plutôplutôt que 1g d’d’acide pour 0,8g de carbonate comme nous faisions précéprécédemment.
3 K2CO3 + 2 C6H8O7 <-> 2 C6H5K3O7 + 3 H2O + 3 CO2
La masse molaire du carbonate de potassium est de 138,2 g/moles et celle de l’l’acide citrique est de de 192,1. Pour refaire l’él’équation en respectant les coefficients, il faut donc 414,6 grammes de carbonates et 384,2 d’d’acide, soit 1g de carbonate et 0,96 d’d’acide pour environ 2 grammes d’d’effervescent. Nous avons calculécalculé pour 2 grammes d’d’effervescents car nous avons vu dans les expéexpériences précéprécédentes que c’éc’était la quantitéquantité la plus adaptéadapté pour le moment.
Nous avons aussi lavélavé l’l’argile-sable de la semaine précéprécédente, et comme le sable est plus gros et sésédimente plus vite, nous avons pu faire un tri granulomégranulométrique àà l’l’eau (malheureusement, nous n’n’avons pas pu conserver tout l’l’argile, uniquement l’l’argile de surface).
Pour cette cinquiècinquième expéexpérience, nous allons donc utiliser ces nouvelles quantitéquantité pour le mémélange effervescent, et garder la meme proportion d’d’argile- sable (1/3 et 2/3). Nous allons cependant mettre du mémélange effervescent partout sur le fond (et non pas que au centre).
Protocole :
bébéchers- cristallisoir
- acide citrique
- carbonate de potassium
- eau
minéminérale - spatule
cuillècuillère- balance
- papier pH
- sable
légèlégèrement humide - argile verte (illite)
- seringue
Nous avons utiliséutilisé 50g d’d’argile pour 100g de sable humide de la semaine précéprécédente.
MéMélange sable-argile : l’l’argile n’n’a pas étéété broyébroyée assez finement, nous avons tout de mêmême essayéessayé comme car : mais le relief en lien avec la réréaction a étéété quelque peu cachécaché par ces gros cailloux de surface.
La façfaçon dont j’j’ai verséversé l’l’eau a aussi laissélaissé une trace en surface : cette expéexpérience éétait un peu un fail.
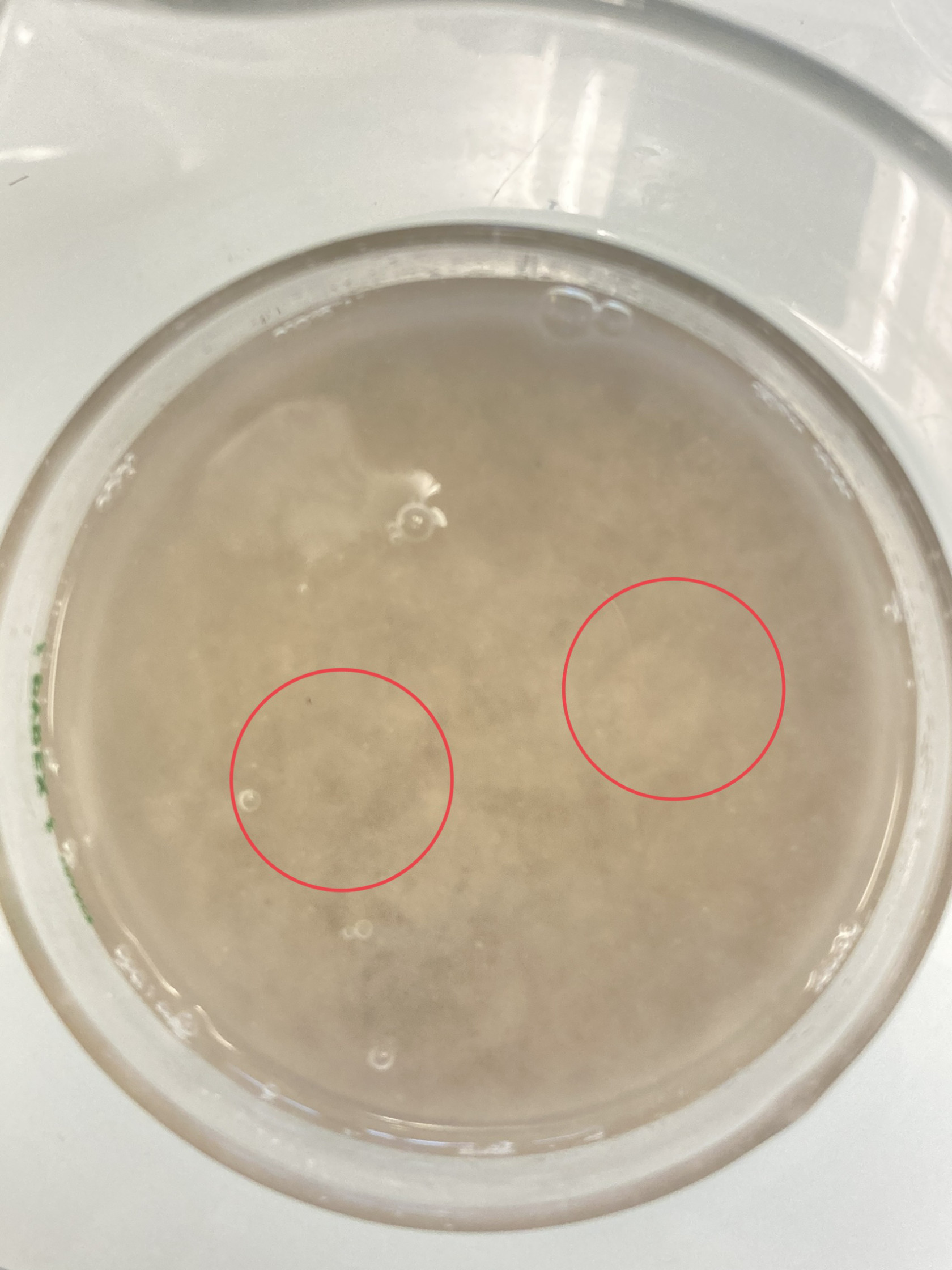
Il n’n’y a cette fois ci sûsûrement pas assez d’d’effervescent ou trop de sésédiments : mêmême si nous avons mis du mémélange effervescent partout sur le fond, nous n’n’avons overseer de cratècratère qu’qu’au centre (2 cratècratères).
Nous avons utiliséutilisé un autre papier pH, qui, avec notre nouvelle ééquation, nous permet d’d’obtenir une réréaction àà pH 7 !
A gauche, pH de l’l’acide citrique. Au centre, pH de l’expél’expérience 5 (àà la fin de l’expél’expérience). A droite, pH du carbonate de potassium.
Pour rérégler le problèproblème de l’l’argile, nous l’l’avons tamisétamisée et nous avons re-broyébroyé les gros cailloux. Nous avons aussi mélangémélangé le reste d’d’argile de la semaine précéprécédente àà notre poudre d’d’argile (recyclage ou quoi).
Pour cette sixièsixième expéexpérience, nous avons doublédoublé les doses de mémélange effervescent (2g de carbonate de potassium et 1,92g d’d’acide citrique).
Nous avons utiliséutilisé :
bébéchers- cristallisoir
- acide citrique
- carbonate de potassium
- eau
minéminérale - spatule
cuillècuillère- balance
- papier pH
- sable
légèlégèrement humide - sable sec
- argile verte (illite)
- seringue
Pour la partie inféinférieure, nous avons mélangémélangé le mémélange effervescent avec 25g de sable humide. Puis, nous avons mis 75g de sable sec et 50g d’d’argile pour la partie supésupérieure. Le problèproblème éétait que sans l’l’argile, le sable humide a déjàdéjà réréagit avec le mémélange effervescent (car avant l’l’argile absorbait l’humiditél’humidité).
Nous avons pu observer un seul cratècratère se former : cela est du peut êêtre au fait que nous n’n’avions pas mis d’d’argile dans la couche inféinférieure et que donc une couche «« de gaz »» s’s’est forméformée entre nos deux couches.
Il serait peut êêtre utile de broyer notre mémélange effervescent : nous nous sommes rendu compte que toutes les billes de carbonate de potassium n’én’étaient pas en contact avec toutes les billes d’d’acide citrique, et que donc a la fin de notre réréaction, lorsque nous mémélangions, la réréaction recommençrecommençait.
Pour cette septièseptième expéexpérience, nous avons utiliséutilisé uniquement du sable sec pour contrer l’l’effet de l’l’effervescent qui commençcommençait avant avec le sable humide. Nous avons aussi mis de l’l’argile partout pout homogénéhomogénéiser les deux couches et pas qu’qu’une couche de gaz se forme entre les deux.
Nous avons utiliséutilisé:
bébéchers- cristallisoir
- acide citrique
- carbonate de potassium
- eau
minéminérale - spatule
cuillècuillère- balance
- papier pH
- sable sec
- argile verte (illite)
- seringue
Nous avons mis 100g de sable sec et 50g d’d’argile. Nous en avons verséversé une petite partie pour faire le fond (avec des l’l’effervescent mélangémélangé) puis le reste par dessus. L’L’effervescent éétait de 2g-1,92g.
CRATÈCRATÈRES !
CRATÈCRATÈRES !
Nous avons toujours ce problèproblème de gaz qui reste coincécoincé, mais tout de mêmême un peu moins.
Pour cette huitièhuitième expéexpérience, nous avons essayéessayé de faire un réréplicat de l’expél’expérience précéprécédente : mêmême quantitéquantité de mémélange effervescent (broyébroyé au mortier), mêmême quantitéquantité d’d’argile-sable, nous avons verséversé l’l’eau de la mêmême façfaçon.
Nous avons utiliséutilisé:
bébéchers- cristallisoir
- acide citrique (1,92g)
- carbonate de potassium (2g)
- eau
minéminérale - spatule
cuillècuillère- balance
- papier pH
- sable sec (100g)
- argile verte (illite) (50g)
- seringue
ProblèProblèmes : L’L’eau a eu du mal a descendre jusqu’jusqu’au mémélange effervescent et nous avons eu pas mal de gaz coincécoincé : peut êêtre utiliser moins d’d’argile la prochaine fois car cela fait une couche trop éétanche, àà la fois pour l’l’eau et pour le gaz.
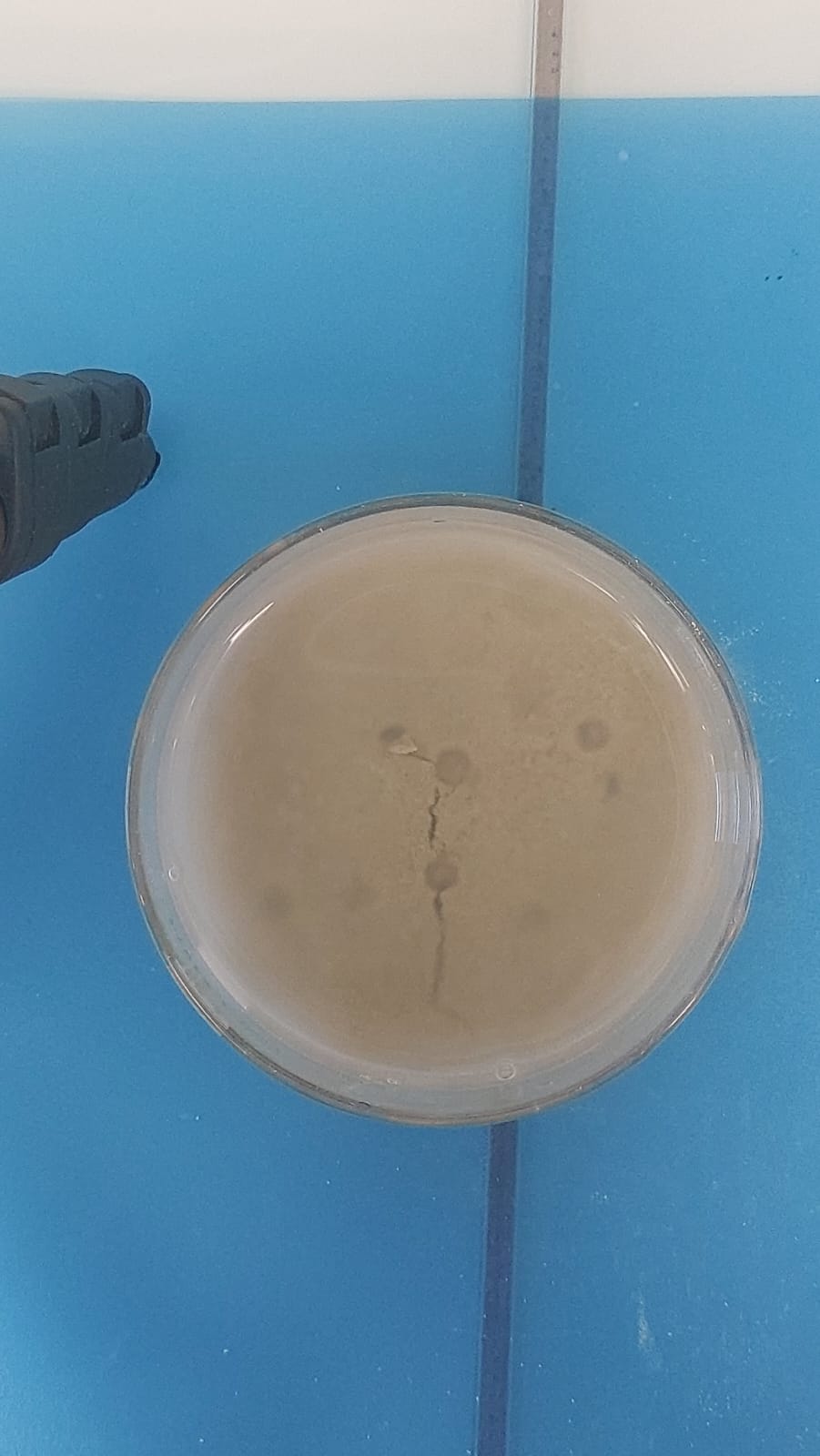
Nous avons tout de mêmême eu quelques cratècratères au dédébut, qui se sont vite transformétransformés en un seul gros cratècratère àà cause du gaz coincécoincé.
Oh tiens gros cratècratère.
01/03/2024 :
Nous avons réréussi àà récupérécupérer le sable d’d’il y a 3 semaines (sable mélangémélangé avec de l’l’argile avec l’l’argile qui a pu êêtre extraite lors de la séséance précéprécédente): 
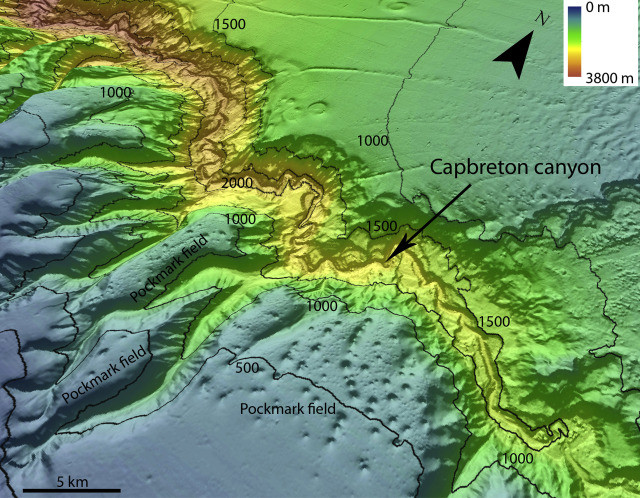
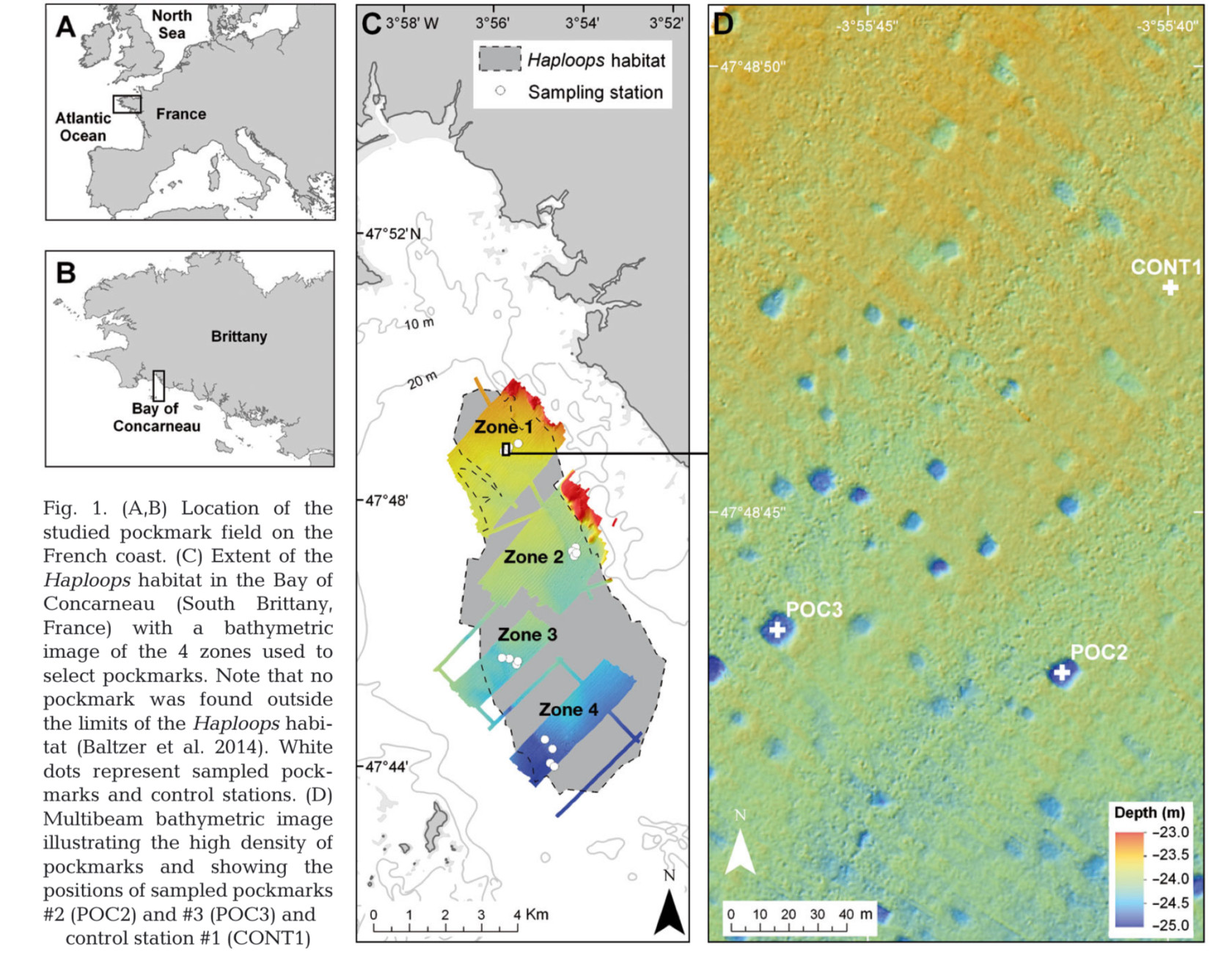
Voici une comparaison entre nos pockmarks et les pockmarks trouvétrouvés dans la nature :
Pockmarks de ARTICLE
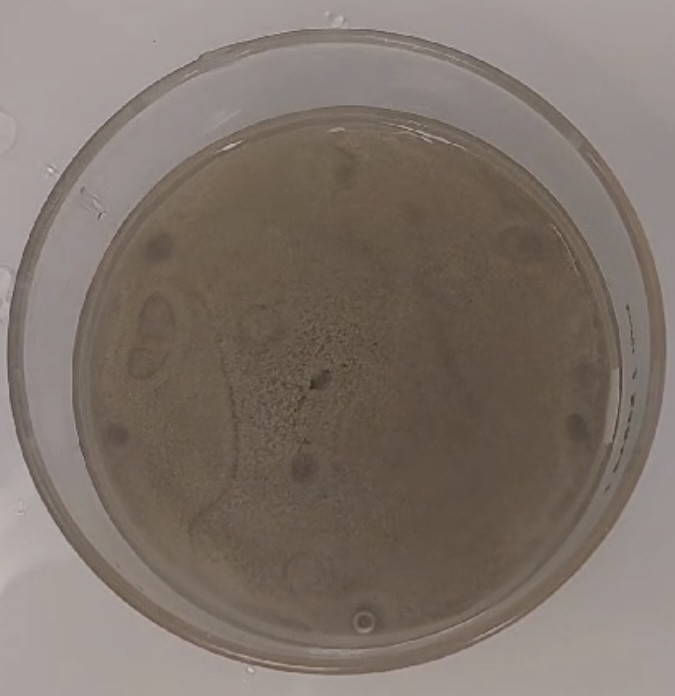
Photo des pockmarks que nous avons obtenus en laboratoire (expéexpérience sept).
En arrivant au labo, nous avons mis a chauffer le mémélange sable-argile de la séséance précéprécédente, pour essayer de récupérécupérer l’l’argile sèsèche d’d’un cotécoté, et le sable de l’l’autre.
Puis, nous avons re-broyébroyé de l’l’argile.
Pour cette neuvièneuvième expéexpérience, nous avons utiliséutilisé 2g carbonate de potassium et 1,92 d’d’acide citrique.
Nous broyons aussi ce mémélange effervescent pour l’homogénél’homogénéiser (ééviter que certains grains de carbonate de potassium et d’d’acide citrique ne se touchent pas).
Nous allons aussi essayer de mettre moins d’d’argile pour contrer la couche de gaz qui se forme : 25g d’d’argile pour 100g de sable.
Nous allons donc faire :
- une couche sable-argile-
mémélange effervescentbroyébroyé - une couche sable-argile
Nous avons utiliséutilisé:
bébéchers- cristallisoir
- acide citrique (1,92g)
- carbonate de potassium (2g)
- eau
minéminérale - spatule
cuillècuillère- balance
- papier pH
- sable sec (100g)
- argile verte (illite) (25g)
- seringue
Nous avons donc fait mis ces deux couches dans un cristallisoir et nous avons verséversé l’l’eau avec la seringue.
Les rérésultats n’én’étaient pas phénoméphénoménaux : nous n’n’avions pas assez d’d’argile pour que les pockmarks tiennent.
ProblèProblème : plus assez d’d’argile. Les bulles n’én’étaient pas trètrès fortes.
La réréaction a étéété neutraliséneutralisée.
Pour cette dixièdixième expéexpérience, nous avons diminuédiminué de 25% les quantitéquantités de sésédiment :
100g de sable -> 75g
50g de sable -> 37,5g
Nous avons utiliséutilisé 2g de carbonate de potassium et 1,92g d’d’acide citrique.
Nous avons fait une couche sable-argile-effervescent et une autre couche plus éépaisse sable-argile.
Nous avons utiliséutilisé:
bébéchers- cristallisoir
- acide citrique (1,92g)
- carbonate de potassium (2g)
- eau
minéminérale - spatule
cuillècuillère- balance
- papier pH
- sable sec (75g)
- argile verte (illite) (37,5g)
- seringue
La quantitéquantité de sésédiment nous semble plutôplutôt correcte, le gaz restait moins coincécoincé (il avait moins de trajet àà remonter).
ProblèProblème : notre méméthode pour verser l’l’eau fait arriver l’l’eau d’d’abord sur les cotécotés. C’C’est donc làlà que se sont forméformés les pockmarks (qui se sont donc forméformés plus vite car ils avaient moins de sésédiment àà remonter). L’L’eau ne descends pas jusqu’jusqu’en bas.
Il faut donc qu’qu’on trouve un moyen pour que l’l’eau soit uniforméuniformément repartie.
La réréaction a étéété neutraliséneutralisée.
Pour cette onzièonzième expéexpérience, nous avons mis 75g de sable et 37,5g d’d’argile. Nous avons mis cependant le double de l’l’effervescent. Nous avons aussi essayéessayé de mieux verser l’l’eau avec la seringue.
Nous avons utiliséutilisé:
bébéchers- cristallisoir
- acide citrique (3,84g)
- carbonate de potassium (4g)
- eau
minéminérale - spatule
cuillècuillère- balance
- papier pH
- sable sec (75g)
- argile verte (illite) (37,5g)
- seringue
Nous avons réréussi àà obtenir de super pockmarks. ProblèProblème : L’L’eau ne s’s’est pas uniforméuniformément réréparti (elle a atteint seulement le centre).
La réréaction àà bien étéété neutraliséneutralisée (papier pH àà 7).
Nous allons essayer de la refaire la semaine prochaine.
Nous avons aussi recyclérecyclé notre argile-sable. La mixture de la séséance précéprécédente que nous avions mis àà sésécher au «« four »» n’n’a pas vraiment bien séchéséché : nous l’l’avons remélangéremélangé àà notre mémélange sable-argile de aujourd’aujourd’hui.
08/03/2024 :
En arrivant au FabLab de GéGéosciences, nous avons vu que l’l’argile et le sable que nous avions laissélaissé sésécher une semaine n’n’ont pas bien séchéséché : nous avons mis àà sésécher au dessiccateur l’l’argile (pendant 2h àà 75°75°C).
Aujourd’Aujourd’hui, nous allons essayer de refaire l’expél’expérience 11.
Pour cette douzièdouzième expéexpérience, nous avons mis 75g de sable et 37,5g d’d’argile, avec un mémélange effervescent àà 4g de carbonate de potassium et 3,84g d’d’acide citrique. Nous avons utiliséutilisé une plus grande seringue (de 60mL). Nous avons aussi récupérérécupéré un trétrépied et une rèrègle pour filmer et faire les mesures.
Nous avons utiliséutilisé :
bébéchers- cristallisoir
- acide citrique (3,84g)
- carbonate de potassium (4g)
- eau
minéminérale - spatule
cuillècuillère- balance
- papier pH
- sable
séchéséchérecyclérecyclé de la semaineprécéprécédente (75g) - argile verte (illite) (37,5g)
- seringue de 60 mL
trétrépiedrèrègle papier
Nous avons broyébroyé le mémélange effervescent. Nous avons mis une couche de sésédiment trètrès fine (pour homogénéhomogénéiser) puis une couche de sésédiment mélangémélangé avec du mémélange effervescent, puis une couche de sésédiment sans effervescent àà nouveau et enfin de l’l’eau (autant d’d’eau que de sésédiment).
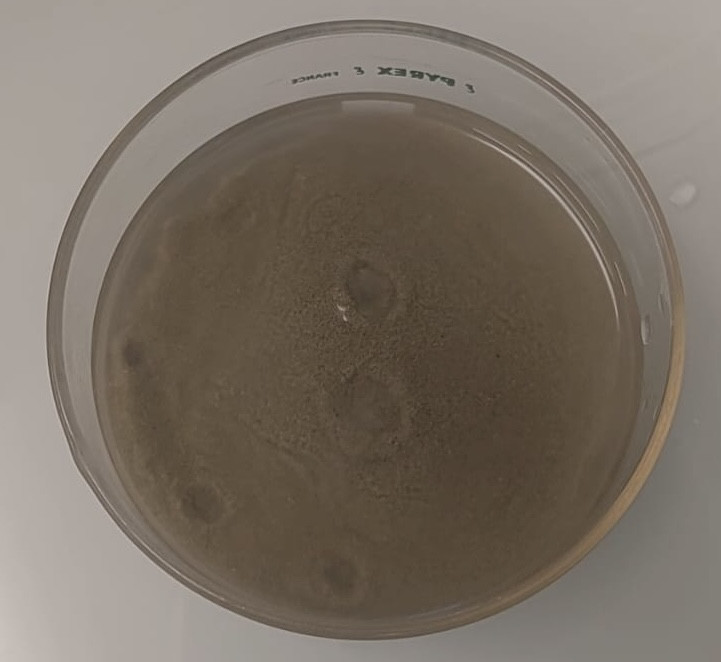
Sable qui commence àà êêtre mouillémouillé par l’l’eau : les pockmarks commencent àà apparaîapparaître.
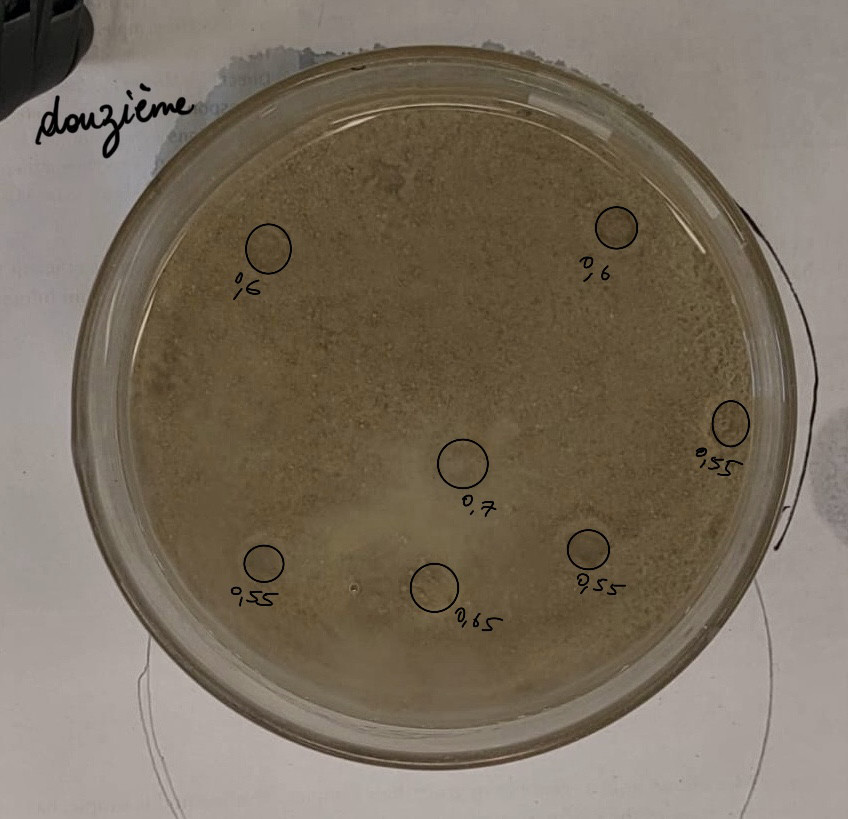
Les pockmarks de l’expél’expérience douze aprèaprès avoir enlevéenlevé l’l’eau.
ProblèProblème : L’L’eau a eu du mal àà atteindre le sésédiment car nous l’l’avions un peu tassétassé (pour mimer le poids de l’l’eau mais fail un peu).
Nous avons mesurémesuré le pH : la réréaction a étéété neutraliséneutralisée.
Pour cette treiziètreizième expéexpérience, nous avons essayéessayé de faire la mêmême chose mais de moins tasser.
Nous avons mis 75g de sable et 37,5g d’d’argile, avec un mémélange effervescent àà 4g de carbonate de potassium et 3,84g d’d’acide citrique.
Nous avons utiliséutilisé :
bébéchers- cristallisoir
- acide citrique (3,84g)
- carbonate de potassium (4g)
- eau
minéminérale - spatule
cuillècuillère- balance
- papier pH
- sable
séchéséchérecyclérecyclé de la semaineprécéprécédente (75g) - argile verte (illite) (37,5g)
- seringue de 60 mL
trétrépiedrèrègle papier
Nous avons broyébroyé le mémélange effervescent. Nous avons mis une couche de sésédiment trètrès fine (pour homogénéhomogénéiser) puis une couche de sésédiment mélangémélangé avec du mémélange effervescent, puis une couche de sésédiment sans effervescent àà nouveau et enfin de l’l’eau (autant d’d’eau que de sésédiment).
ProblèProblème : Cette fois ci, l’l’eau s’s’est mal rérépartie : l’l’eau va d’d’abord sur les cotécotés et donc c’c’est làlà que les pockmarks se sont forméformés.
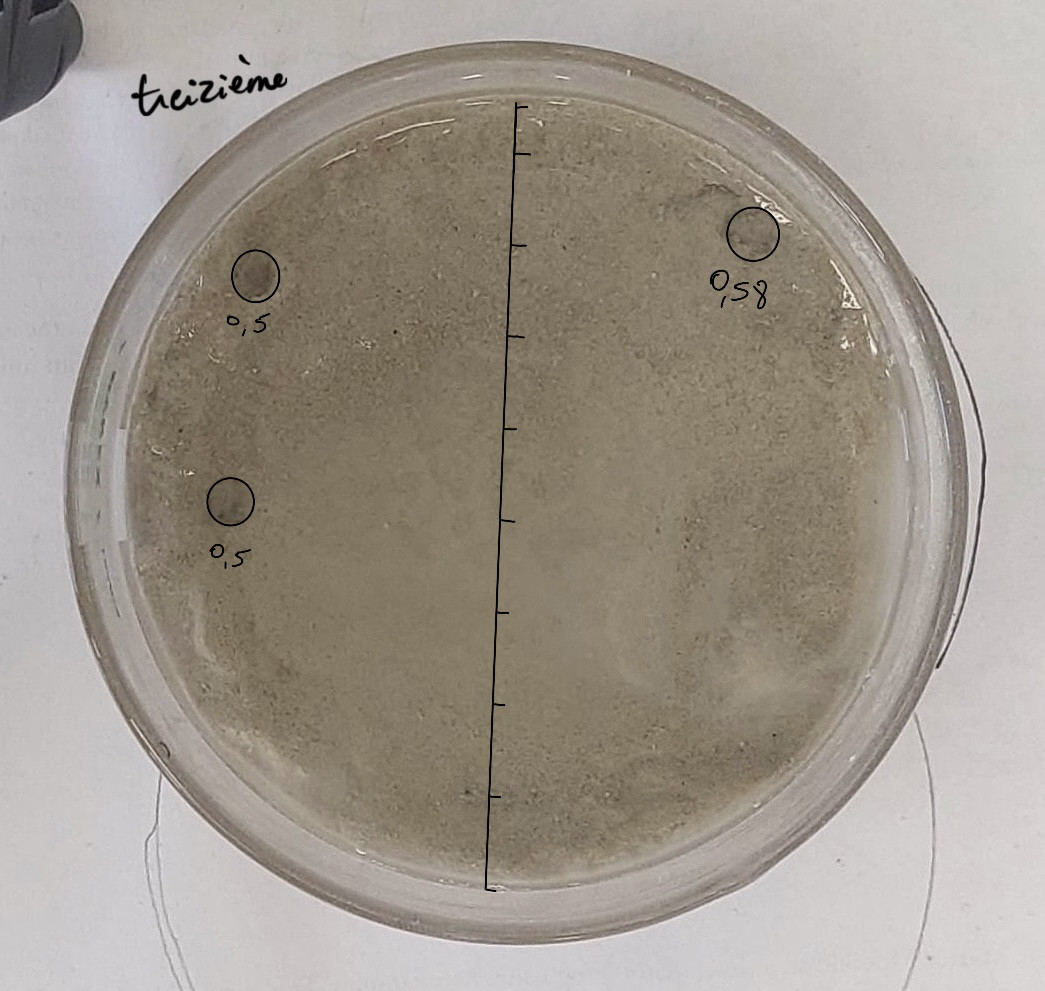
Pockmarks de l’expél’expérience 13 : les pockmarks sont sur le cotécoté.
Pour cette quatorzièquatorzième expéexpérience, nous avons mis l’l’effervescent au centre, pour ééviter les pockmarks sur les cotécotés (sur les cotécotés, ils sont trop écraséécrasés et donc mesurer leur diamèdiamètre est compliquécompliqué. Nous avons broyébroyé le mémélange effervescent. Nous avons mis une couche de sésédiment trètrès fine (pour homogénéhomogénéiser) puis une couche de sésédiment mélangémélangé avec du mémélange effervescent (au centre) et du mémélange sable-argile sur le pourtour, puis une couche de sésédiment sans effervescent àà nouveau et enfin de l’l’eau (autant d’d’eau que de sésédiment).
Nous avons utiliséutilisé :
bébéchers- cristallisoir
- acide citrique (3,84g)
- carbonate de potassium (4g)
- eau
minéminérale - spatule
cuillècuillère- balance
- papier pH
- sable
séchéséchérecyclérecyclé de la semaineprécéprécédente (75g) - argile verte (illite) (37,5g)
- seringue de 60 mL
trétrépiedrèrègle papier
MéMélange sable-argile+ mémélange effervescent au centre et sable-argile sur les pourtour.
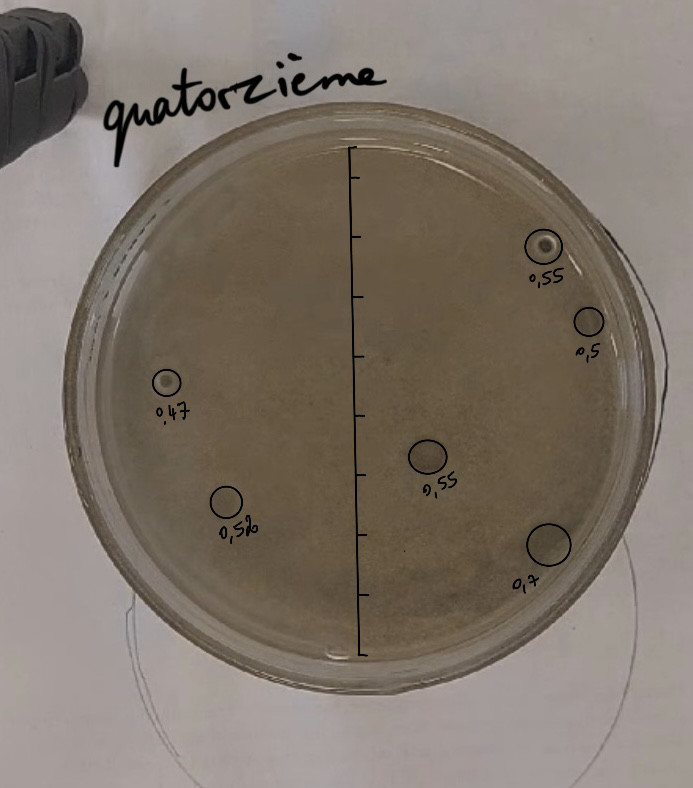
Nous avons moins tassétassé, mais l’l’eau àà toujours eu du mal àà aller jusqu’jusqu’en bas. On observe des pockmarks sur les cotécotés tout le mêmême.
La réréaction a étéété neutraliséneutralisée.
Une fois retournéretournées au FabLab de GéGéosciences, nous avons pu retrouver l’l’argile que nous avons laissélaissé 3h au dessiccateur àà 75°75°C. 
L’L’argile est - presque- pure : nous pouvons donc la réréutiliser. Il reste àà nettoyer l’l’eau.
15/03/2024 :
Nous avons commencécommencé par aller au FabLab de GéGéosciences pour voir si le mémélange argile-sable avait séchéséché. Et en effet, nous avons pu retirer l’l’argile qui s’s’est décollédécollée du sable. 
Nous l’l’avons ensuite mélangémélangé àà l’l’argile que nous avions aussi récupérérécupéré en la dessicant la semaine dernièdernière et nous les avons broyébroyé pour retrouvéretrouvé de l’l’argile prêprête àà l’l’emploi !
Puis, nous avons lavélavé le sable (dans lequel il restait un tout petit peu d’d’argile, mais qui n’én’était pas réréutilisable) et laissélaissé àà sésécher.
Ensuite, nous nous sommes rendues au FabLab de Biologie, nous nous avons assembléassemblé le trétrépied pour filmer les expéexpériences. Pour toujours filmer nos expéexpériences sous le mêmême angle, nous avons préparépréparé un repèrepère en plastique, avec deux cercles pour les pieds du trétrépied, et un grand pour le cristallisoir. En effet, la semaine passépassée, de l’l’eau éétait tombétombée sur notre repèrepère en papier, et l’l’avait déformédéformé. Afin d’éd’éviter de nouveau de problèproblème, nous en avons fait un en plastique. 
Nous pouvons passer àà une nouvelles expéexpérience, oùoù nous allons reproduire les expéexpériences de la semaine dernièdernière pour avoir des replicas pour ensuite éétudier le diamèdiamètre des pockmarks. Nous allons calculer le diamèdiamètre en fonction de la hauteur de sésédiment.
Pour cette quinzièquinzième expéexpérience, nous utilisons de d’d’argile recyclérecyclée et du sable (non recyclérecyclé). Nous avons broyébroyé le mémélange effervescent. Nous avons mis une couche de sésédiment trètrès fine (pour homogénéhomogénéiser) puis une couche de sésédiment mélangémélangé avec du mémélange effervescent et enfin une couche de sésédiment sans effervescent. Nous avons ajoutéajouté de l’l’eau avec la seringue (autant d’d’eau que de sésédiment).
Nous avons utiliséutilisé :
bébéchers- cristallisoir
- acide citrique (3,84g)
- carbonate de potassium (4g)
- eau
minéminérale - spatule
cuillècuillère- balance
- papier pH
- sable (75g)
- argile verte
recyclérecyclée desséséancesprécéprécédentes (illite) (37,5g) - seringue de 60 mL
trétrépiedrèrègle papier
Notre sésédiment fait 1,5 cm de haut environ. Nous avons essayéessayé de mettre autant d’d’eau que de sésédiment. Mais le problèproblème est que l’l’eau a toujours du mal àà infiltrer correctement le sésédiment et la réréaction n’n’a pas pu se faire entièentièrement. 
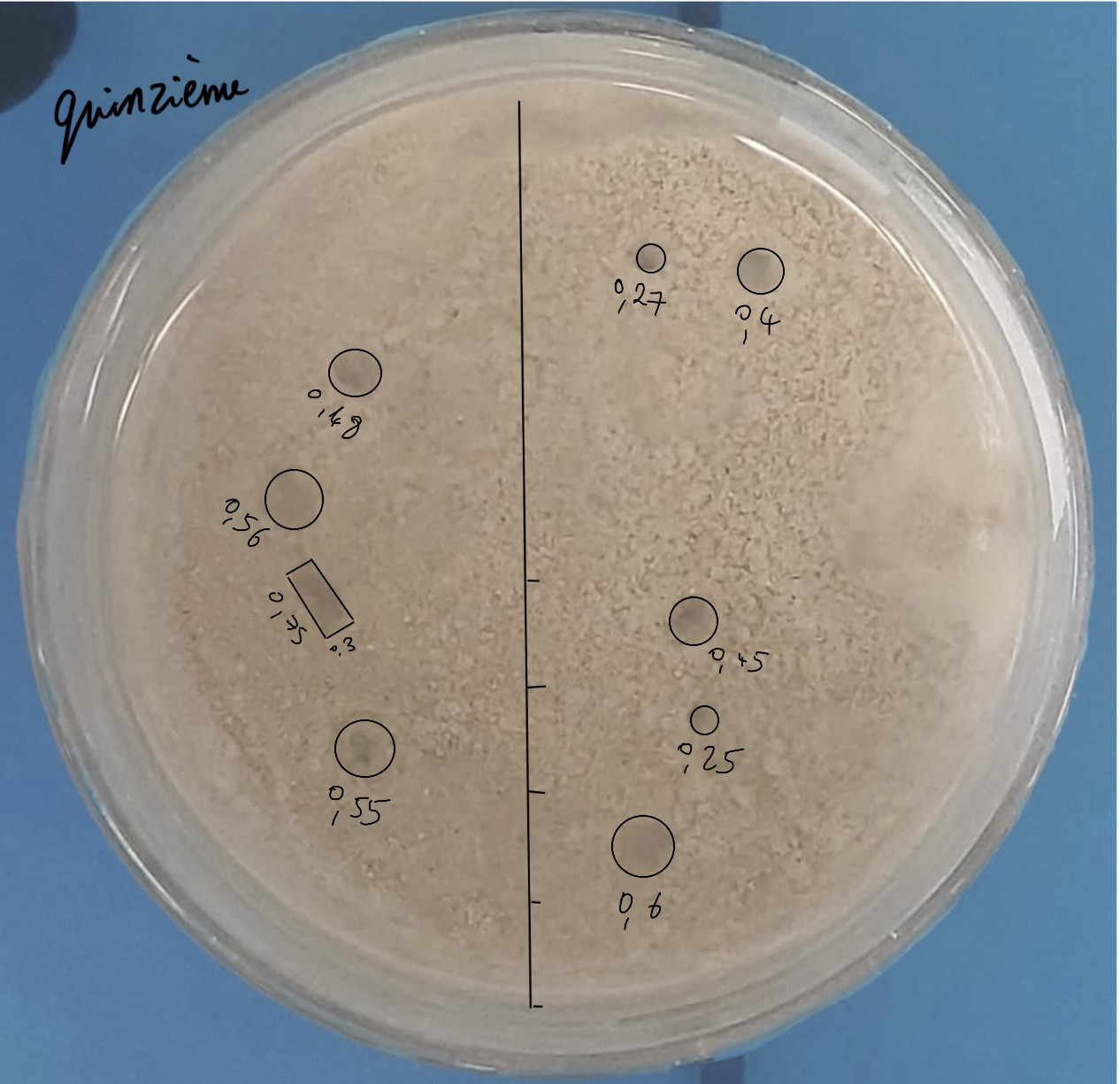
Les pockmarks sont un peu flous mais nous en avons eu beaucoup.
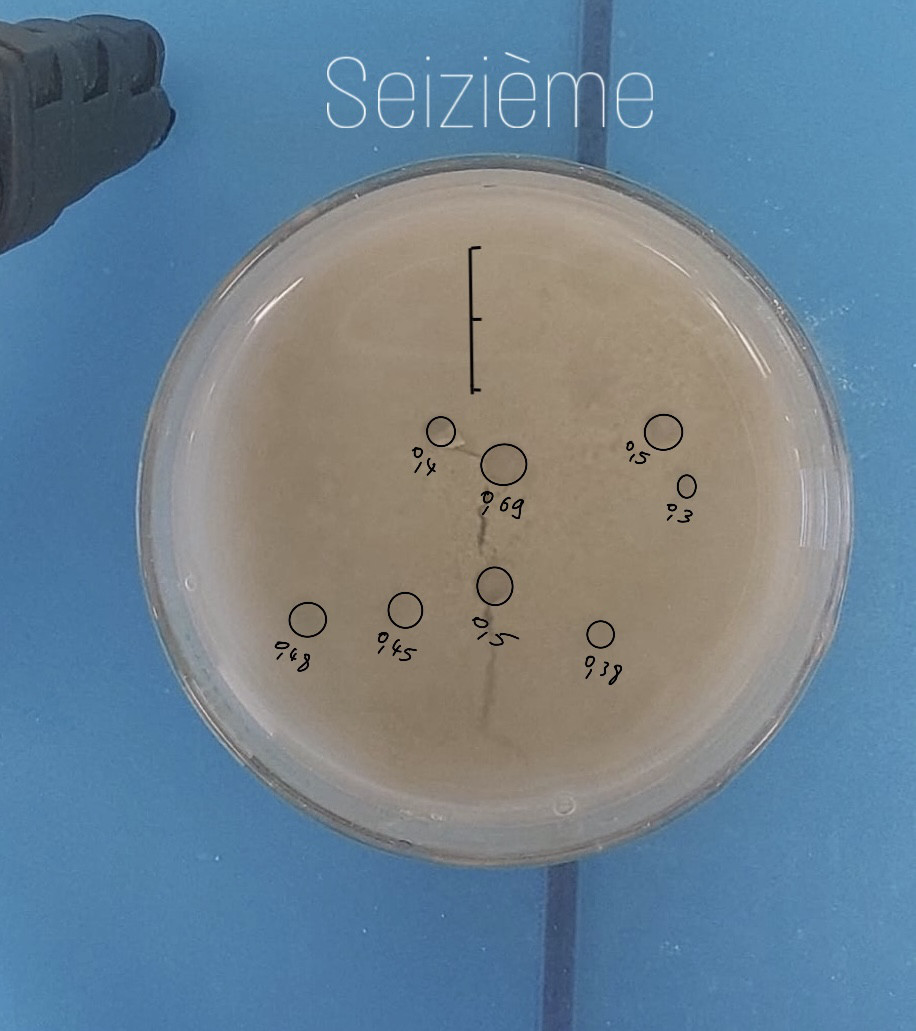
Pour cette seizièseizième expéexpérience, nous utilisons de d’d’argile recyclérecyclée et du sable (non recyclérecyclé). Nous avons broyébroyé le mémélange effervescent. Nous avons mis une couche de sésédiment trètrès fine (pour homogénéhomogénéiser) puis une couche de sésédiment mélangémélangé avec du mémélange effervescent et enfin une couche de sésédiment sans effervescent. Nous avons ajoutéajouté de l’l’eau avec la seringue (autant d’d’eau que de sésédiment).
Nous avons utiliséutilisé :
bébéchers- cristallisoir
- acide citrique (3,84g)
- carbonate de potassium (4g)
- eau
minéminérale - spatule
cuillècuillère- balance
- papier pH
- sable (75g)
- argile verte
recyclérecyclée desséséancesprécéprécédentes (illite) (37,5g) - seringue de 60 mL
trétrépiedrèrègle papier- maryse
Nous avons eu l'idéidée d'utiliser dédésormais une maryse pour vider et nettoyer les bébéchers et le cristallisoir lors de nos expéexpériences. En effet, le sable rayait fortement les verreries et produisait un bruit trètrès désagrédésagréable. Nous avons fait exactement la mêmême expéexpérience que précéprécédemment. Le sésédiment éétait aussi aux alentours de 1,5 - 1,6 cm.
Avec nos diverses photos, nous pouvons maintenant calculer le diamèdiamètre et la densitédensité des pockmarks.
Nous avons pu voir que les expéexpériences 1, 2, 3, 4, 5, et 9 ne sont pas exploitables.
En revanche, les 6, 7, 8, 10, 11, 12, 13, 14, 15, 16 sont exploitables pour mesurer et observer des pockmarks !
22/03/2024 :
Nous avons commencécommencé par vider l'eau stagnante au dessus de notre mémélange sable-argile, afin que celui-ci soit sec pour la prochaine semaine. Nous avons ensuite mis àà sésécher notre argile que nous avons fait dédécanter, sans sable, dans le dessiccateur àà 75°75°C pour 3 heures.
Nous sommes ensuite passépassées aux calculs de proportion de pockmarks par rapport àà la surface totale du cristallisoir. Le cristallisoir ayant un diamèdiamètre de 8,5 cm, son rayon est de 4,25 cm ou 42,5 mm.
Son aire est donc éégale àà (42,5)²²*ππ = 5674,5mm²5mm²
Calculs proportion expéexpérience 6 :
Un seul pockmarks de 8mm de diamèdiamètre, avec un diamètre moyen de 8mm :
4²4²*ππ= 50,3mm²3mm²
50,3/5674,5*100= 0,89% de surface couverte par les pockmarks pour l'expéexpérience 6.
Aire moyenne des pockmarks : 50,3 mm²mm²
Calculs proportion expéexpérience 7 :
Quatre pockmarks de 3, 8, 4, et 5.5 mm de diamèdiamètre, avec un diamètre moyen de 5,125mm :
1->1.5²5²*ππ= 7mm²7mm²
2->4²4²*ππ= 50.3mm²3mm²
3->2²2²*ππ= 12.6mm²6mm²
4->2,75²75²*ππ= 23.75mm²75mm²
7+50.3+12.6+23.75=93.65mm²65mm² de pockmarks.
93.65/5674.5*100= 1.65% de surface occupéoccupée par les pockmarks.
Aire moyenne des pockmarks : 93.65/4 = 23,41 mm²mm²
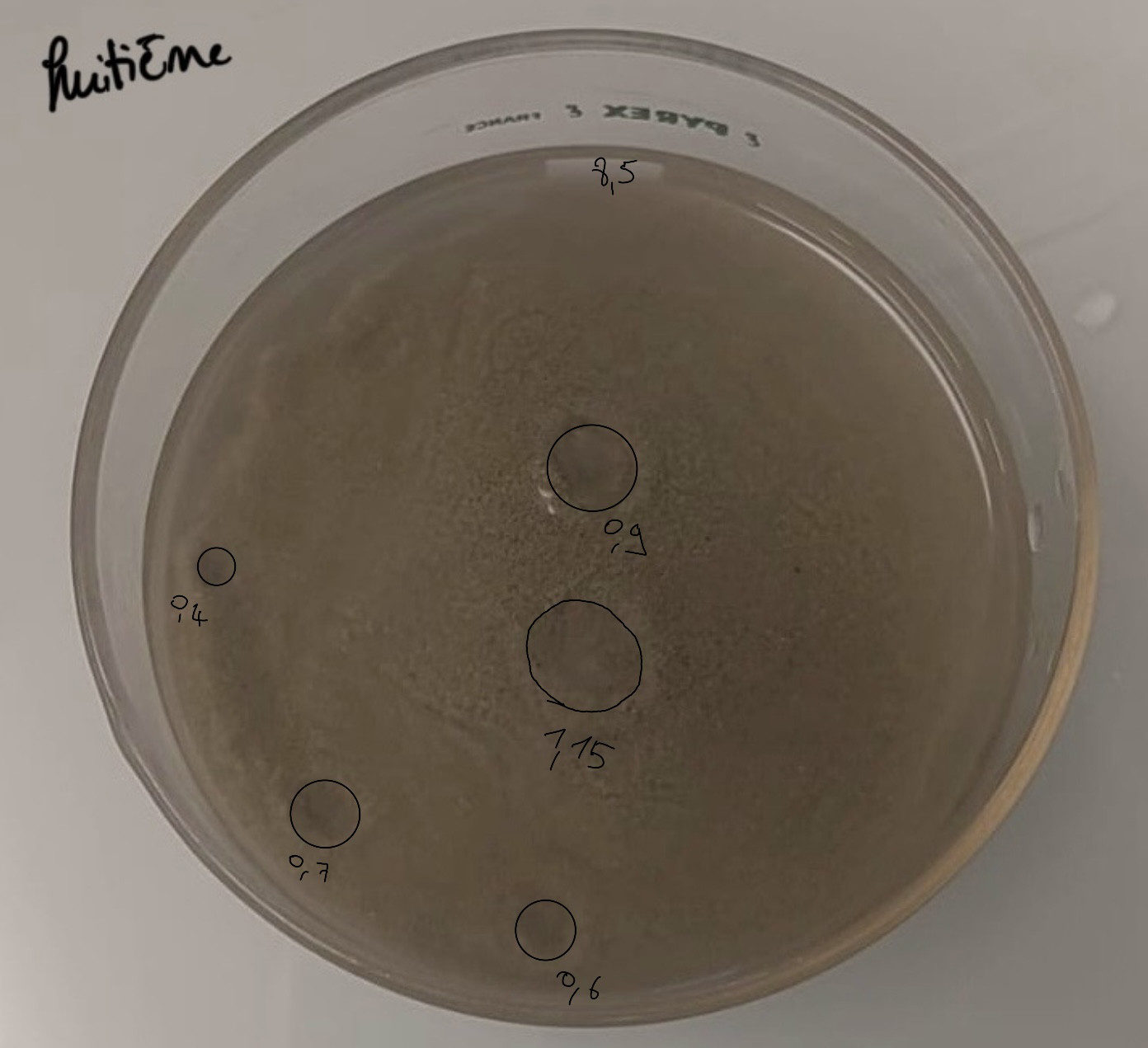
Calculs proportion expéexpérience 8 :
Cinq pockmarks de 9, 4, 7, 11.5, et 6 mm de diamèdiamètre :
1->4.5²5²*ππ= 63.61mm²61mm²
2->2²2²*ππ= 12.6mm²6mm²
3->3.5²5²*ππ= 38.48mm²48mm²
4->5.75²75²*ππ= 103.87mm²87mm²
5->3²3²*ππ= 28.27mm²27mm²
63.61+12.6+38.48+103.87+28.27=246.83mm²83mm² de pockmarks.
246.83/5674.5*100= 4.35% de surface occupéoccupée par les pockmarks.
Aire moyenne des pockmarks : 246,83/5 = 49,37mm²mm²
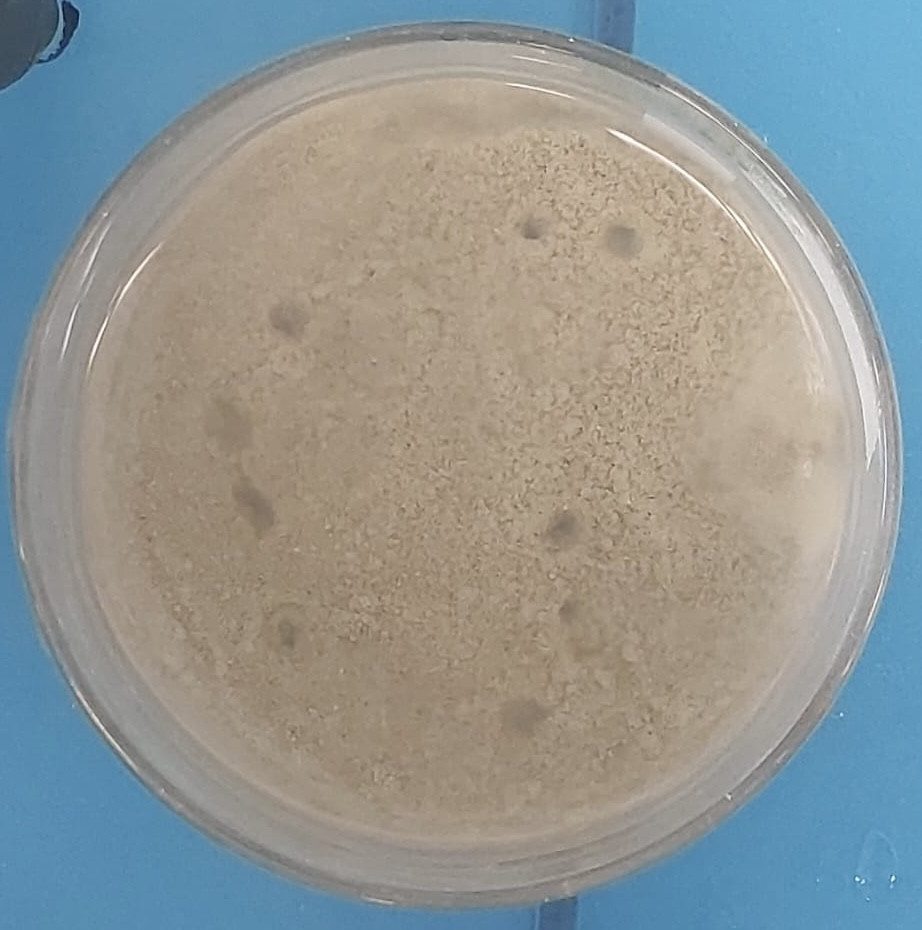
Calculs proportion expéexpérience 10 :
Dix pockmarks de 5, 5, 5, 6, 6, 4, 4, 4.5, et 7mm de diamèdiamètre et un avec une forme particulièparticulière ressemblant àà un rectangle de 15*5 mm de cotécoté.
1->2,5²5²*ππ= 19.63mm²63mm²
2->2,5²5²*ππ= 19.63mm²63mm²
3->2,5²5²*ππ= 19.63mm²63mm²
4->3²3²*ππ= 28.27mm²27mm²
5->3²3²*ππ= 28.27mm²27mm²
6->2²2²*ππ=12.57mm²57mm²
7->2²2²*ππ=12.57mm²57mm²
8->2.25²25²*ππ=15.90mm²90mm²
9->3.5²5²*ππ=38.48mm²48mm²
10->15*5=75mm²75mm² car respecte plus la forme d'un rectangle.
19.63+19.63+19.63+28.27+28.27+12.57+12.57+15.90+38.48+75=269.95mm²95mm² de pockmarks.
269.95/5674.5*100= 4.76% de surface occupéoccupée par les pockmarks.
Aire moyenne des pockmarks : 269,95/10 = 26,995 mm²mm²
Calculs proportion expéexpérience 11 :
Il y a 3 pockmarks de 4, 6, et 7.5 mm de diamèdiamètre :
1 -> 2²2²*ππ = 12,57 mm²mm²
2 -> 3²3²*ππ = 28,27 mm²mm²
3 -> 3,75²75²*ππ = 44,18 mm²mm²
12,57 + 28,27 + 44,18 = 85,02 mm²mm²
85,02/5674,5 * 100 = 1,5 % de surface occupéoccupée par les pockmarks.
Aire moyenne des pockmarks : 85,02/3 = 28,34 mm²mm²
Calculs proportion expéexpérience 12 :
Il y a 7 pockmarks de 6, 6, 7, 5.5, 5.5, 5.5, et 6.5 mm de diamèdiamètre :
1 -> 3²3²*ππ = 28,27 mm²mm²
2 -> 3²3²*ππ = 28,27 mm²mm²
3 -> 3,5²5²*ππ = 38,48 mm²mm²
4 -> 2,75²75²*ππ = 23,76 mm²mm²
5 -> 2,75²75²*ππ = 23,76 mm²mm²
6 -> 3,25²25²*ππ = 33,18 mm²mm²
7 -> 2,75²75²*ππ = 23,76 mm²mm²
28,27 + 28,27 + 38,48 + 23,76 + 23,76 + 33,18 + 23,76 = 199,48 mm²mm²
199,48/5674,5 * 100 = 3,52 % de surface occupéoccupée par les pockmarks.
Aire moyenne des pockmarks : 199,48/7 = 28,49 mm²mm²
Calculs proportion expéexpérience 13 :
Il y a 3 pockmarks de 5, 5, 5.8 mm de diamèdiamètre :
1 -> 8,5²5²*ππ = 19,63 mm²mm²
2 -> 2,5²5²*ππ = 19,63 mm²mm²
3 -> 2,9²9²*ππ = 26,42 mm²mm²
19,63 + 19,63 + 26,42 = 65,68 mm²mm²
65,68/5674,5 * 100 = 1,16 % de surface occupéoccupée par les pockmarks.
Aire moyenne des pockmarks : 65,68/3 = 21,89 mm²mm²
Calculs proportion expéexpérience 14 :
Il y a 6 pockmarks de 4.7, 5.2, 5.5, 5.5, 5, et 7 mm de diamèdiamètre :
1 -> 2,35²35²*ππ = 17,35 mm²mm²
2 -> 2,6²6²*ππ = 21,24 mm²mm²
3 -> 2,75²75²*ππ = 23,76 mm²mm²
4 -> 2,75²75²*ππ = 23,76 mm²mm²
5 -> 2,5²5²*ππ = 19,63 mm²mm²
6 -> 3,5²5²*ππ = 38,48 mm²mm²
17,35 + 21,24 + 23,76 + 23,76 + 19,63 + 38,48 = 144,22 mm²mm²
144,22/ 5674,5 * 100 = 2,54 % de surface occupéoccupée par les pockmarks.
Aire moyenne des pockmarks : 144,22/6 = 24,03 mm²mm²
Calculs proportions expéexpérience 15 :
Il y a 9 pockmarks de 2.7, 4, 4.5, 2.5, 6, 5.5, 5.6, 4.8, et un pockmark rectangulaire de 7,5x3 mm :
1 -> 1,35²35²*ππ = 5,73 mm²mm²
2 -> 2²2²*ππ = 12,57 mm²mm²
3 -> 2,25²25²*ππ = 15,9 mm²mm²
4 -> 1,25²25²*ππ = 4,91 mm²mm²
5 -> 3²3²*ππ = 28,27 mm²mm²
6 -> 2,75²75²*ππ = 23,76 mm²mm²
7 -> 2,8²8²*ππ = 24,63 mm²mm²
8 -> 2,4²4²*ππ = 18,09 mm²mm²
9 -> 7,5*3 = 22,5 mm²mm²
5,73 + 12,57 + 15,9 + 4,91 + 28,27 + 23,76 + 24,63 + 18,09 + 22,5 = 156,36 mm²mm²
156,36/5674,5 * 100 = 2,755 % de surface occupéoccupée par les pockmarks.
Aire moyenne des pockmarks : 156,36/9 = 17,37 mm²mm²
Calculs proportion expéexpérience 16 :
Il y a 8 pockmarks de 5, 3, 4, 6.9, 5, 3.8, 4.5 et 4.8 mm de diamèdiamètre :
1 -> 2,5²5²*ππ = 19,63 mm²mm²
2 -> 1,5²5²*ππ = 7,06 mm²mm²
3 -> 2²2²*ππ = 12,57 mm²mm²
4 -> 3,45²45²*ππ = 37,39 mm²mm²
5 -> 2,5²5²*ππ = 19,63 mm²mm²
6 -> 1,9²9²*ππ = 11,34 mm²mm²
7 -> 2,25²25²*ππ = 15,9 mm²mm²
8 -> 2,4²4²*ππ = 18,09 mm²mm²
19,63 + 7,06 + 12,57 + 37,39 + 19,63 + 11,34 + 15,9 + 18,09 = 141,61 mm²mm²
141,61/5674,5 * 100 = 2,49 % de surface occupéoccupée par les pockmarks.
Aire moyenne des pockmarks : 141,61/8 = 17,7
Nous obtenons un diamètre moyen de pockmarks de 5,798mm.
Nous avons ensuite voulu comparer ces donnédonnées avec des donnédonnées de la littélittérature :
«« Role of pockmarks in diversity and species assemblages of coastal macrobenthic communities »» - Dubois et al. (2015).
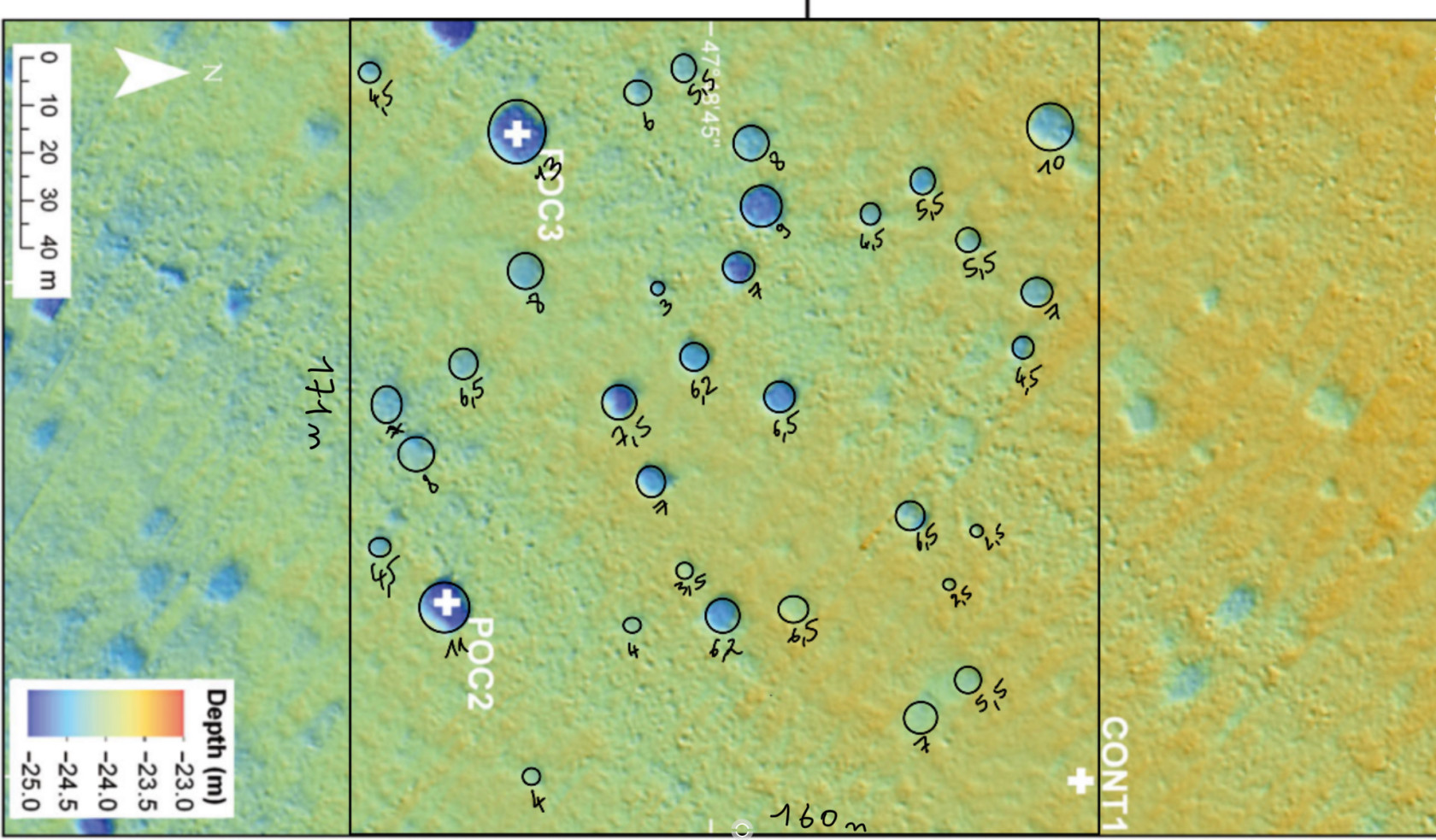
Nous avons utiliséutilisé une image de pockmarks de Dubois et al. 2015, et nous avons utiliséutilisé la mêmême méméthode que pour nos expéexpériences.
Le carrécarré que nous avons sélectionnésélectionné fait 171x160 m = 27 360 m²m²
Il y a 34 pockmarks
1 -> 7m -> 38,48m²48m²
2-> 5,5m -> 23,76m²76m²
3-> 2,5m -> 4,91m²91m²
4-> 2,5m -> 4,91m²91m²
5-> 4m -> 12,57m²57m²
6-> 11m -> 95,03m²03m²
7-> 4m -> 12,57m²57m²
8-> 6,2m -> 30,19m²19m²
9-> 3,5m -> 9,62m²62m²
10-> 6,5m -> 33,18m²18m²
11-> 6,5m -> 33,18m²18m²
12-> 8m -> 50,3m²3m²
13-> 4,5m -> 13,9m²9m²
14-> 7m -> 38,48m²48m²
15-> 7,5m -> 44,18m²18m²
16-> 7m -> 38,48m²48m²
17-> 6,5m -> 33,18m²18m²
18-> 8m -> 50,3m²3m²
19-> 6,5m -> 33,18m²18m²
20-> 6,2m -> 33,18m²18m²
21-> 3m -> 7,06m²06m²
22-> 7m -> 38,48m²48m²
23-> 4,5m -> 15,9m²9m²
24-> 7m -> 38,48m²48m²
25-> 9m -> 63,62m²62m²
26-> 8m -> 50,3m²3m²
27-> 4,5m -> 15,9m²9m²
28-> 4,5m -> 15,9m²9m²
29-> 5,5m -> 23,76m²76m²
30-> 5,5m -> 23,76m²76m²
31-> 10m -> 78,53m²53m²
32-> 5,5m -> 23,76m²76m²
33-> 6m -> 28,27m²27m²
34-> 13m -> 137,73m²73m²
La surface recouverte de pockmarks est de 1105,56m²56m².
1105,56/27 360 * 100 = 4,04% de surface occupéoccupée par les pockmarks.
On peut voir qu’qu’on est un peu dans les mêmêmes ordres de grandeurs. Malheureusement, c’c’est car, dans la nature, les pockmarks sont trètrès nombreux et petits proportionnellement àà nos expéexpériences modèles:modèles.
29/03/2024 :
Nous avons recyclé le mélange sable-argile que vous avions laissé la semaine dernière.
Puis, nous nous sommes renseigné sur les pockmarks « naturels » et les nôtres, et nous avons essayé de voir si notre modèle est analogue à ce que nous trouvons. Malheureusement, il nous manque beaucoup de données.
Nous avions vu la semaine dernière que nos pockmarks étaient plus gros et moins nombreux que dans la nature. C’est peut être lié à la nature et à la profondeur de notre sédiment.
En effet, nous avons un mélange sable-argile. Nous sommes arrivés à une proportion de 1 part de sable pour 1/2 part d’argile car si nous mettons trop d’argile, l’eau ne circule plus, et si nous n’en mettons pas assez, les pockmarks ne se forment pas.
Nous allons essayer de faire varier la hauteur de sédiment pour voir si cela va impacter la taille de nos pockmarks.
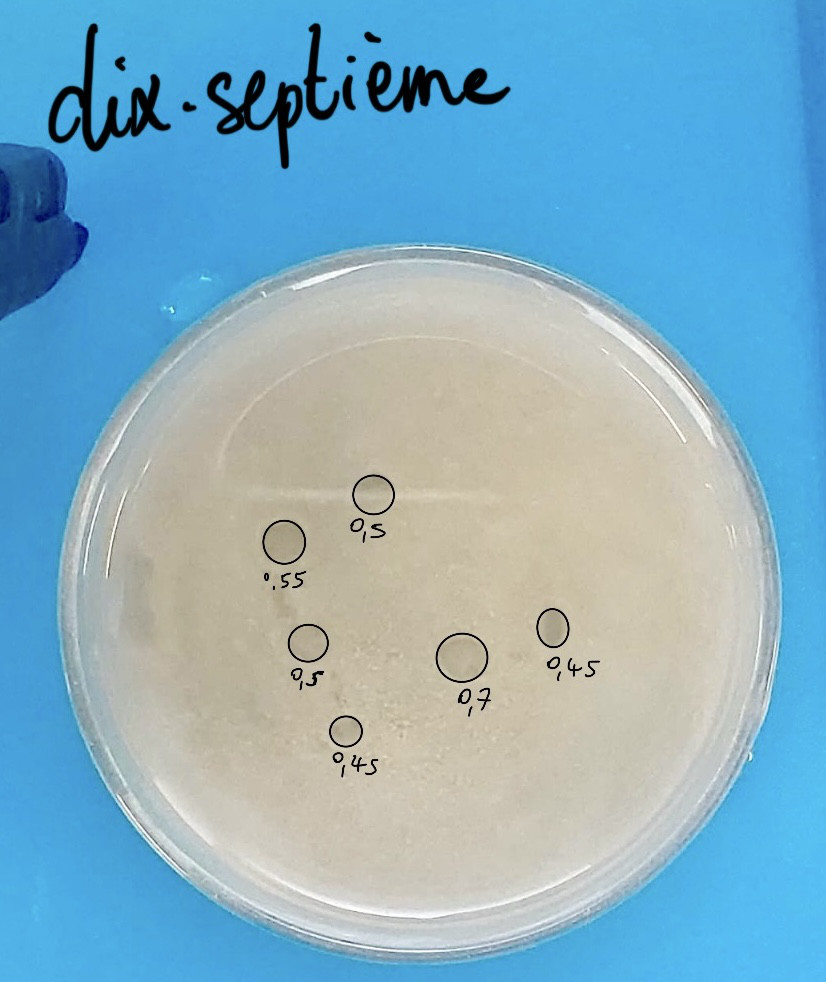
Pour cette dix-septième expérience, nous avons essayé d’avoir une hauteur de cm de 2cm, contre 1,5cm habituellement. Nous avons donc ajouté x0,25 notre sédiment pour avoir 0,25 fois plus de sédiment : nous nous retrouvons avec environ 2cm de sédiment.
Nous avons utilisé :
- béchers
- cristallisoir
- acide citrique (3,84g)
- carbonate de potassium (4g)
- eau minérale
- spatule
- cuillère
- balance
- papier pH
- sable (75 + 18,75 = 93,75 g)
- argile verte recyclée des séances précédentes (illite) (37,5 + 9,375= 46,875g)
- seringue de 60 mL
- trépied
- règle papier
- maryse
Nous avons obtenu ni plus ni moins de pockmarks que pour les expériences précédentes : nous en avons 6, alors que en moyenne nous avons 5,6 pockmarks par expérience. Les pockmarks de cette expérience ont un diamètre moyen de 5,2mm (contre 5,798mm). Ajouter du sédiment n’a pas réduit le nombre de pockmarks ni agrandit la taille.
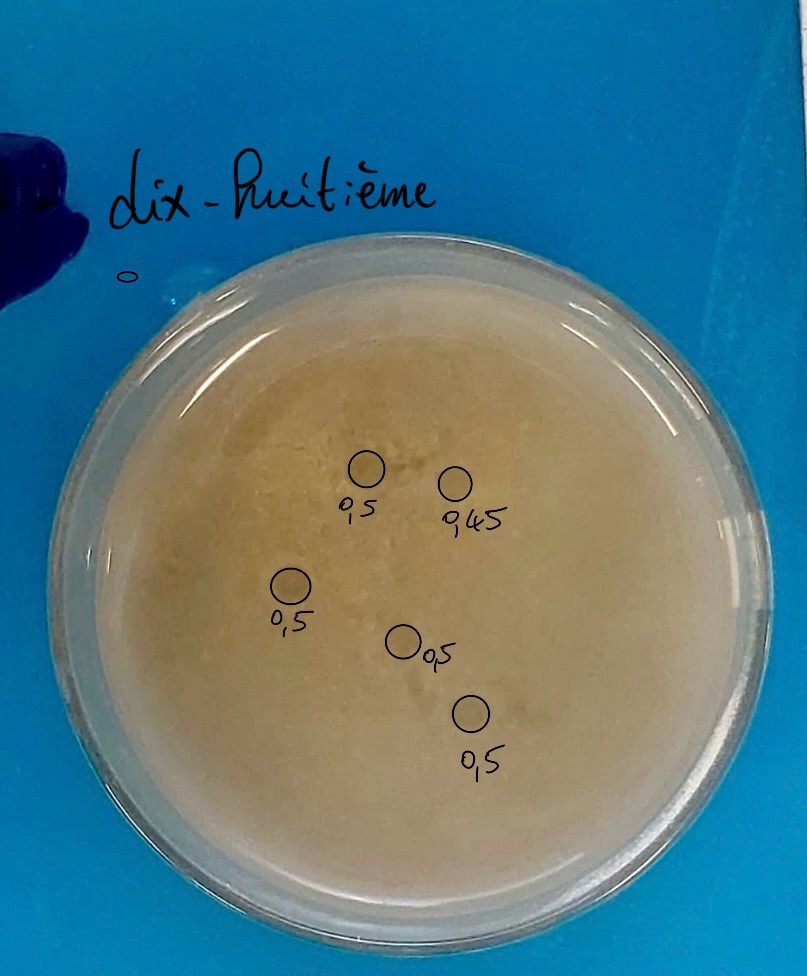
Pour cette dix-huitième expérience, nous avons mis 0,25 fois moins de sédiment, pour avoir 1cm de sédiment. C’est ce que nous avons obtenu.
Nous avons utilisé :
- béchers
- cristallisoir
- acide citrique (3,84g)
- carbonate de potassium (4g)
- eau minérale
- spatule
- cuillère
- balance
- papier pH
- sable (75-18,75 = 56,25g)
- argile verte recyclée des séances précédentes (illite) (37,5- 9,375 = 28,125g)
- seringue de 60 mL
- trépied
- règle papier
- maryse
Nous avons obtenu ni plus ni moins de pockmarks que pour les expériences précédentes : nous en avons 5, alors que en moyenne nous avons 5,6 pockmarks par expérience. Les pockmarks de cette expérience ont un diamètre moyen de 4,9mm (contre 5,798mm). Enlever du sédiment n’a pas augmenté le nombre de pockmarks, cela a peut être un peu diminué leur taille.