Création d’encre ferro-gallique
Qu’est ce que l’encre ferro-gallique :
Cette encre médiévale s’appelle une encre ferro-gallique, cela est du aux sels métalliques (sulfate de fer) qui entrent dans sa composition. Il est nécessaire de manipuler ces sels métalliques avec précautions en mettant des gants, car ils sont irritant pour la peau. La plupart des ingrédients nécessaire à la fabrication de l’encre métallo-gallique sont trouvables chez un droguiste.
Les Egyptiens connaissaient déjà la réaction des sels de fer sur les extraits de galles. Mais il faut attendre le moyen-âge pour que l'encre ferro gallique se répande en Europe, au point de devenir le véhicule de toutes les écritures durant huit cents ans. Elle est appréciée pour sa facilité de fabrication et sa stabilité. On possède des manuscrits vieux de dix siècles écrits avec cette encre : elle n'a rien perdu de sa noirceur.
Jusque vers 1850 c'est l'encre unique que l'on utilise en France. Les dessinateurs, en particulier, s'en servent pour le trait et pour le lavis, en concurrence avec le bistre, la sépia et plus tard l'encre de chine (beaucoup plus visqueuse). Indélébile, très fluide, elle est appréciée pour les écritures officielles : c'est
« l'encre de l'état civil » du XIX° siècle. Le résidu de la filtration forme une boue noire qui servait au marquage des emballages militaires et des tonneaux. En 1974 elle était encore utilisée en Allemagne pour certaines écritures administratives.
Ingrédients :
- 1 unité de noix de galle / d’acide tannique
- 1 unité de gomme arabique
- 1 unité de sulfate de fer
- 48 cl d’eau de pluie ou d’eau distillée
1) Les noix de galle (acide gallotannique)
Les noix de galles sont des croissances sphériques trouvées sur les chênes. Leur développement est
déclenché lorsque les insectes perforent des branches d'arbre et des brindilles là où ils déposent
ensuite leurs œufs. Lorsque les larves éclosent, elles se nourrissent de l'arbre et sécrètent un irritant.
Les galls sont le mécanisme de défense de la plante. Au fur et à mesure qu'elles grandissent, elles
fournissent un abri et de la nourriture aux larves jusqu'à leur maturité et sont capables de mâcher
leur chemin.
Les noix de galle sont utilisés comme source des tanins - des polyphénols qui peuvent être extraits
de diverses parties de plantes (écorce, feuilles, gousses, fruits, noix ). Le tanin peut également être
extrait d'autres sources telles que le bois ou l'écorce de châtaignier, de chêne, de Sumach, des
grenades.
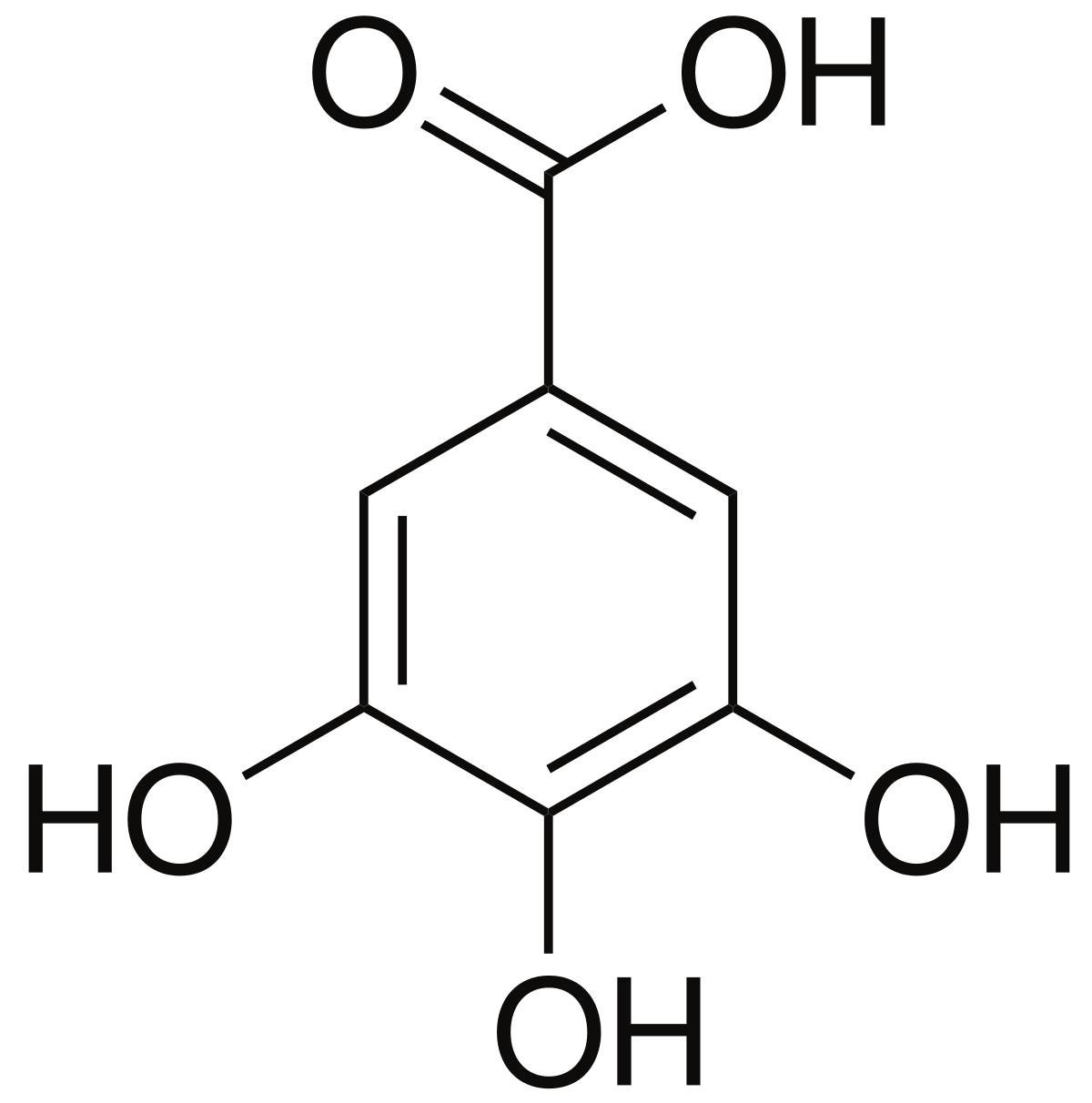
L'acide gallotannique est le type de tanin, et ce sont les groupes d'acide gallique dans l'acide
gallo-annique qui réagissent avec le sulfate de fer pour créer le complexe tanate ferrique coloré.
L'hydrolyse de l'acide gallotannique pour produire de l'acide gallique et de l'eau peut être
réalisée en utilisant des acides ou en laissant fermenter la solution de tanin .
2) Le sulfate de fer II ou sulfate ferreux - FeSO4*7H2O
Utilisé comme source de fer. En mélangeant du tanin avec du sulfate de fer, un complexe
soluble dans l'eau se forme. Du fait de sa solubilité, l'encre est capable de pénétrer la surface
du papier, ce qui rend difficile l'effacement. Lorsqu'il est exposé à l'air, il se transforme en
un tannate ferrique, qui est un pigment plus foncé pas soluble dans l'eau, ce qui contribue
à sa permanence en encre d'écriture.Le processus d'obscurcissement de l'encre est dû à l'oxydation des ions de fer (Fe 2+) à (Fe3+) par l'oxygène de l'air. Pour cette raison, l'encre liquide doit être stockée dans un flacon bien arrêté, et
devient souvent inutilisable après un certain temps.
3) Gomme arabique
Il est utilisé comme liant en encres et en peintures et peut être trouvé sous forme de grumeaux
transparents allant du jaune pâle à l'orange.
La gomme arabique sert de nombreux objectifs dans une encre: elle rend l'encre plus visible,
améliorant son écoulement à partir du stylo; elle maintient les particules pigmentaires insolubles en
suspension; elle aide à lier l'encre à la surface d'écriture; et elle donne plus de brillance et de
profondeur de l'encre.
Matériel nécessaire à la manipulation :
- Balance
- Mortier et pilon
- Bécher
- Plaque chauffante
Protocole :
Il faut commencer par piller les noix de galle en petits morceaux, puis mettre ces morceaux dans une casserole avec l’eau de pluie.
Mettre ensuite ce mélange à bouillir, jusqu’à ce que la quantité d’eau soit réduite de moitié.
Ensuite après avoir laisser refroidir, il faut filtrer le mélange à travers un linge, puis le remettre sur le feu.
Une fois que le mélange recommence à bouillir, mettre la gomme arabique pilée et attendre qu’elle se dissolve en mélangeant.
Il faut ensuite ajouter sulfate de fer, et remuer quelques secondes.
Enfin, il faut retirer le mélange du feu et bien le mélanger pour que tout les ingrédients soit bien dissous.
Laisser ensuite l’encre à l’air libre dans la casserole pendant une nuit, ce qui la rendra plus brillante et plus noire .
Le lendemain, il faudra filtrer l’encre dans un morceau de tissus, puis la mettre dans un flacon ou une bouteille hermétique.
L’encre est maintenant prête à être utilisée !
La chimie derrière la création de l’encre ferro-gallique :
Les encres ferro-galliques sont des préparations élaborées, comportant bien entendu du fer, mais aussi des tanins, ces substances organiques que l’on trouve dans de très nombreux végétaux : pépins de raisins ou écorces de chêne ; on les retrouve typiquement dans le vin, mais aussi le thé. Un exemple de précurseur de tanin bien connu est l’acide gallique, un dérivé du phénol présent dans la noix de galle, d’où le nom « ferro-gallique » donné à l’encre.
La recette générale des encres ferro-galliques est la suivante : on prend de l’extrait de noix de galle, ce qui revient à en récupérer l’acide gallique et on le mélange avec du sulfate de fer. On obtient un précipité noir qui peut alors être utilisé comme encre. Que se passe-t-il chimiquement? Il se produit en fait une réaction entre l’acide gallique et les ions Fe2+ du sulfate de fer, qui, en présence de l’oxygène ambiant, conduisent à une oxydation de Fe2+ en ions Fe3+, avec la formation d’un complexe dit binucléaire.
Déjà connue dans l’Antiquité et très répandue au Moyen Âge, cette recette s’est affinée au cours du temps par l’ajout d’un « liant » tel que la gomme arabique, dont le rôle est d’ajuster la viscosité de l’encre et faciliter l’écriture.



No Comments