Fiche technique : réactions organiques simples
Cette page a été écrite en reprenant le contenu du cours du LU2Ci002, chimie organique 1, de Ludovic Jullien, Giovanni Poli et Serge Thorimbert de l'année universitaire 2020-2021 à Sorbonne Université.
Introduction
Cette page a pour but de vous introduire la chimie organique, à travers quelques réactions simples, la substitution nucléophile (SN) et l'élimination (E), sur des fonctions monovalentes. Ces fonctions correspondent à une famille d'espèces chimiques, où la fonction comporte un atome X (ou un groupe d'atomes) électronégatif directement lié à l'atome de carbone C tétraédrique. Cette fonction peut être un halogène (Cl, Br, I), un alcool (OH) ou amine (NR1R2).
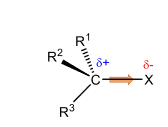 Schéma d'une molécule possédant une fonction monovalente
Schéma d'une molécule possédant une fonction monovalente
Afin de simplifier les choses, nous allons nous focaliser sur les dérivés halogénés (X = Hal).
Substitution nucléophile
Il existe deux types de substitution nucléophile, la SN2 et la SN1. La substitution nucléophile se fait en présence d'un nucléophile Y-, possédant au moins un doublet non liant. Elle s'effectue en une étape au cours de laquelle la formation de la liaison C-Y et la rupture de la liaison X-C ont lieu en même temps et un état de transition est observé dans le cas de la SN2. Tandis que pour la SN1, ces deux étapes se font successivement, indépendamment l'une de l'autre.
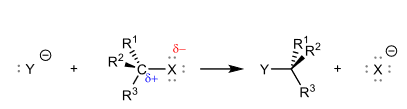 Bilan réactionnel d'une substitution nucléophile sur un dérivé halogéné
Bilan réactionnel d'une substitution nucléophile sur un dérivé halogéné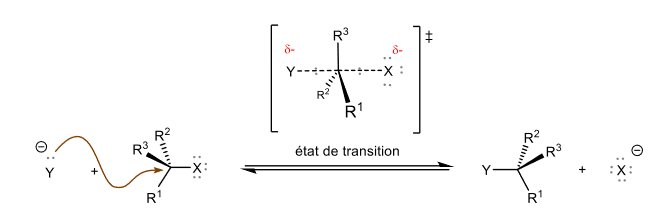 Mécanisme réactionnel d'une SN2 sur un dérivé halogéné
Mécanisme réactionnel d'une SN2 sur un dérivé halogéné
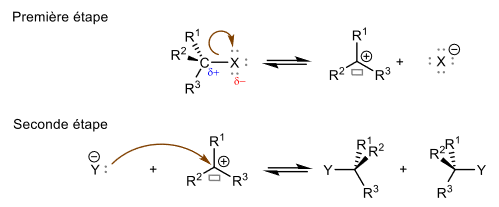
Mécanisme réactionnel d'une SN1 sur un dérivé halogéné
Élimination
Tous les nucléophiles n'entrainent pas de réactions de substitution, il peut arriver de faire face à une élimination à la place, notamment lorsqu'il est basique B-. Le dérivé halogéné est éliminé pour former une double liaison carbone-carbone. Il existe trois types d'élimination, la E2, la E1 et la E1cB.
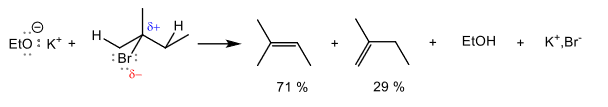 Exemple de réaction d'élimination (l'alcène obtenu le plus majoritaire correspond à celui qui est le plus substitué c'est-à-dire avec le moins d'atomes d'hydrogène sur la double liaison)
Exemple de réaction d'élimination (l'alcène obtenu le plus majoritaire correspond à celui qui est le plus substitué c'est-à-dire avec le moins d'atomes d'hydrogène sur la double liaison)
Semblable à la SN2, la E2 se fait une unique étape au cours de laquelle la formation de la double liaison C=C et la rupture des liaisons C-H et C-X ont lieu simultanément.
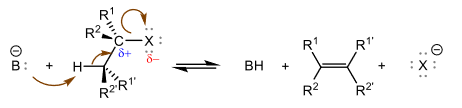 Mécanisme réactionnel d'une E2
Mécanisme réactionnel d'une E2
Pour les E1 et E1cB, on observe deux étapes. Lors de la E1, un carbocation est formé, à l'issue de la rupture de la liaison C-X. La seconde étape constitue simultanément la rupture de la liaison C-H et la formation de la liaison C=C. Tandis que pour la E1cB, la rupture de la liaison C-H se fait en premier pour formé en carbanion, qui réagit ensuite pour former la liaison C=C et rompre la liaison C-X.
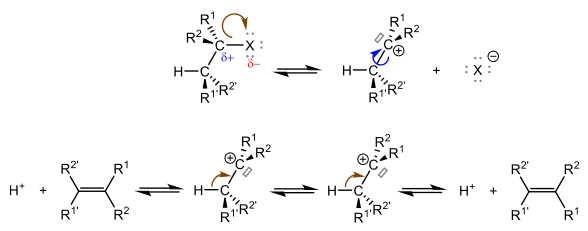 Mécanisme d'une E1 sur un dérivé halogéné. La libre rotation de la liaison C-C du carbocation détermine l'obtention possible de deux dérivés éthyléniques.
Mécanisme d'une E1 sur un dérivé halogéné. La libre rotation de la liaison C-C du carbocation détermine l'obtention possible de deux dérivés éthyléniques.
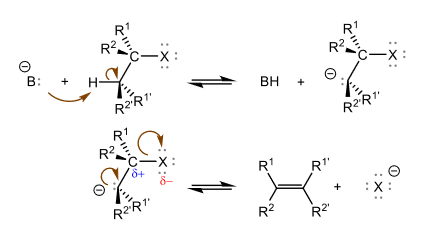
Mécanisme d'une E1cB sur un dérivé halogéné.
No Comments