Etude de la corrélation entre la concentration en flavonoïdes dans les parties ariennes de la carotte et tolérance à Alternaria dauci
Dosage des flavonoïdes dans les feuilles de carottes en condition de stress hydrique et en condition témoin
Protocole :
Introduction :
L'une des méthodes les plus répandues pour la détermination de la quantité en flavonoïdes dans les extraits végétaux est le dosage colorimétrique au chlorure d'aluminium, où l'ion Al3+ est utilisé comme agent complexant. Les groupements oxo et hydroxyles en ortho présents sur le cycle aromatique B de la plupart des flavonoïdes permettent au trichlorure d’aluminium de chélater ces molécules. Ils forment ainsi des complexes colorés jaune absorbant dans l’UV-Vis.
Réactifs et matériels :
- Chlorure d’aluminium hexahydraté (solution 2 % w/v).
- Quercétine (standard, HPLC)
- Eau purifiée (Milli-Q).
- Vortex
- Evaporateur rotatif
- Bain à ultrasons (chauffant si possible) (sonicateur) pouvant être branché et rentrer sous une hotte
- Centrifugeuse
- Dessiccateur sous vide (supportant l’évaporation de l’éthanol)
- Spectrophotomètre UV-Vis (500–800–2 nm) — réglé à 420 nm.
Réplicats biologiques et techniques
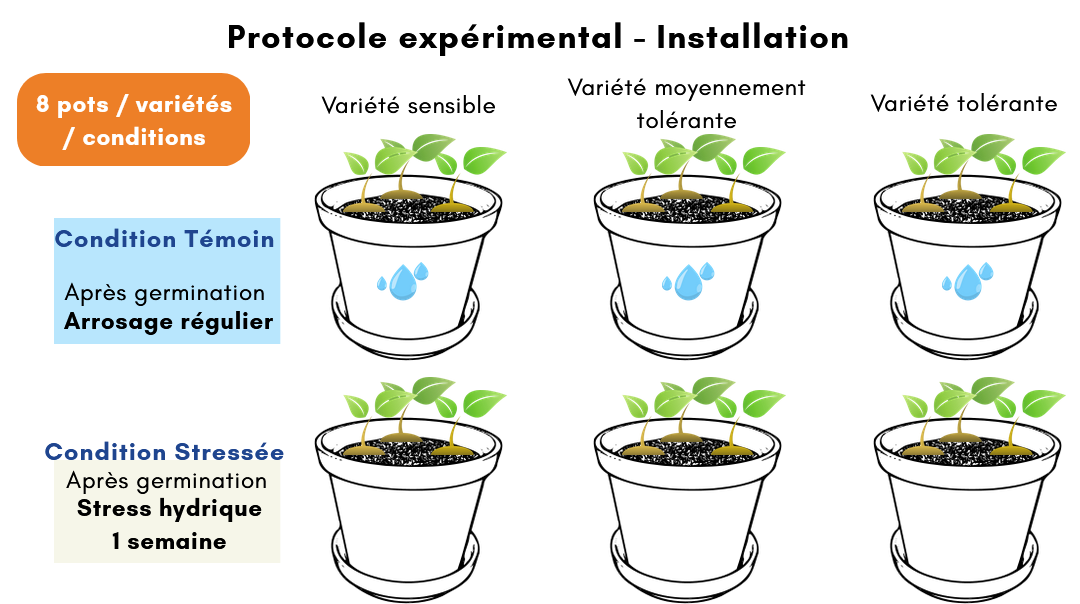
Matériel végétal et conditions de croissance :
3 variétés de carottes sont utilisées comme matériel végétal. Une variété sensible à Alternaria Dauci (variété VS), une est tolérante (variété VT), et une est à tolérance modérée (variété VMT).
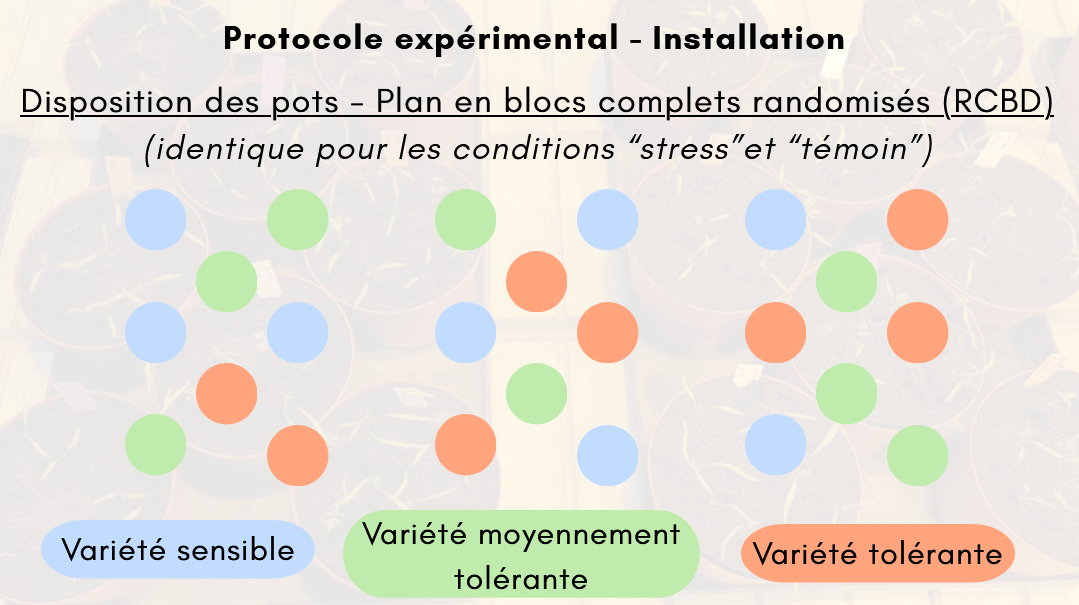
Dans la serre, les semis sont réalisés en petits pots (ou alvéoles). Après un stade de développement adéquat, les plants vigoureux sont sélectionnés et repiqués dans des pots de 2L pour la poursuite de la culture. Ces pots sont disposés sur un ou plusieurs tablars dans la serre. Quatre plantules de carottes seront repiquées dans chaque pot. Puis, au bout de trois semaines de croissance à dater du semis, ces pots sont divisés en deux catégories qui suivent deux traitements différents. Pour la première catégorie (témoin T), les carottes continuent d’être correctement arrosées, les conditions de croissance ne changent pas. Pour la seconde catégorie (stress hydrique H) , un stress hydrique est infligé aux plantules par arrêt de l’’irrigation des carottes pendant 7 jours. Pour chaque modalité (variété & T ou H), 8 pots sont réalisés.
Plants de carottes avant stress hydrique (à gauche) et après 7 jours sans arrosage (à droite)
Prélèvement des feuilles pour le dosage
Pour l’analyse colorimétrique des flavonoïdes totaux (méthode AlCl₃), des feuilles seront prélevées sur les plantes issues des quatre pots dédiés au dosage pour chacune des modalités expérimentales (six variétés × deux conditions hydriques). Deux dates d’échantillonnage sont retenues : le jour 0, correspondant à l’état avant l’application du stress hydrique, et le jour 7, correspondant à la fin de la période de stress. Ces deux points de mesure permettront d’évaluer l’évolution de la teneur foliaire en flavonoïdes au cours du stress hydrique et de comparer la réponse des différentes variétés de carottes.
Suivi cinétique in vivo de la teneur foliaire en flavonoïdes chez les différentes variétés de carotte
Sur 16 plantes différentes pour la même modalité (4 plantules, provenant de 4 pots), et mesurer la teneur en flavonoïdes d’une feuille grâce à la pince multi-pigment MPM 100 au jour J0, J2, J4, J6, J7. Pour chaque jour, calculer la moyenne de l’ensemble des mesures. Tracer l’évolution de cette moyenne au cours du temps pour chaque modalité.
Lyophilisation et broyage des feuilles
-
Lyophilisation des feuilles avec un lyophilisateur
-
Broyage des feuilles sèches avec un pilon et un mortier
Evaluation du stress hydrique :
Mesure de la perte d’eau dans les pots :
Les pots soumis à un stress hydrique seront pesés à T = 0, puis régulièrement jusqu’à atteindre un certain pourcentage de perte de masse, correspondant à la perte de masse hydrique. Le stress hydrique, donc l’expérience, cesse dès que tous les pots ont atteint ce même pourcentage de perte.
Les pots non soumis à un stress hydrique devraient maintenir leur masse durant toute la durée de l’expérience.
Mesure de la perte d’eau dans les feuilles :
Les feuilles prélevées pour le dosage colorimétrique seront pesées avant d’être lyophilisées (obtention de la masse fraîche), puis après avoir très lyophilisées et réduite en poudre (obtention de la masse sèche). La variation du rapport masse sèche/masse fraîche entre le début et la fin de l’expérience indiquera la perte de masse hydrique, et donc représentera le niveau de stress hydrique subi par ces plantules.
Extraction des flavonoïdes de la matière sèche végétale
Méthode 1 :
-
Préparer un Falcon 15mL contenant 5 mL d’éthanol 95% (v/v)
-
Placer le Falcon dans un agitateur incubateur réglé sur 40°C (et pré-conditionné)
-
Laisser incuber pendant une quinzaine de minutes
-
Sortir le tube et vérifier à l’aide d’une sonde thermomètre que la température du solvant est à 40°C
-
Le cas échéant, ajouter 0.15 g de matière végétale séchée et broyée.
-
Laisser la solution macérer à 40 °C pendant 10 min dans l’agitateur incubateur.

-
Répéter l’extraction 3 fois (centrifuger le Falcon (Centrifuger à 3 000 × g pendant 10 min) , récupérer le surnageant, et rajouter 5 mL de solution neuve d’éthanol à 95%, ce deux fois) puis regrouper les filtrats. dans un ballon (monocol).
-
A l’aide de l’évaporateur rotatif, évaporer le solvant à 50 °C sous pression réduite (150 mbar) jusqu’à obtenir l’extrait sec.
-
On évapore jusqu’à ce qu’il reste environ 1mL de solvant qu’on transfère dans une coupelle. On rince le ballon fois fois avec 0.5 mL de EtOH 95% de solvant pour tout récupérer et on rajoute cet éthanol de rinçage dans la coupelle. Puis, on place la coupelle dans un dessiccateur sous vide à 30-40°C pendant une quinzaine de minutes. Transférer l’extrait sec dans un vial ambré prépeser. Peser le vial. Sécher pendant une dizaine de minutes. Repeser le vial pour vérifier que l’extrait est complètement sec (masse constante).
-
Conserver l’extrait sec pour analyses ultérieures.
Dosage colorimétrique
Préparation des échantillons pour le dosage colorimétrique
-
Préparer un Falcon 15mL contenant 5.0 mL de méthanol (100%).
-
Peser 10–50 mg de l’extrait sec dans une coupelle
-
Ajouter l’extrait sec dans le Falcon contenant le méthanol.
-
Dans un bain à ultrasons pré-conditionné à 40°C placé sous la hotte, placer le Falcon sur un support, et dévisser le bouchon à moitié.
-
Soniquer pendant 45 min.
-
Centrifuger à 3 000 × g pendant 10 min.
-
Recueillir le surnageant clair dans un flacon ambré — c’est la solution d’échantillon prête pour le dosage.
Préparation des étalons
-
Préparer la solution mère de quercétine : dans un tube Eppendorf (2mL) dissoudre 5,0 mg de quercétine dans 1,0 mL de méthanol (solution mère = 50 mg/mL).
-
Préparer des étalons par dilutions en méthanol pour obtenir la gamme 5 – 200 µg/mL.
Ne pas oublier de faire le blanc entre chaque étalon. Pour faire le blanc, préparer un tube contenant le solvant et le réactif selon la même proportion (0,6 mL solvant + 0,6 mL AlCl₃ 2 %) et l’utiliser pour la correction spectrale.
Réaction colorimétrique
-
Dans un tube Eppendorf (2mL), placer 0,6 mL de solution étalon ou de l’échantillon
-
Ajouter 0,6 mL de solution de chlorure d’aluminium 2 %.
-
Mélanger doucement (vortex bref).
-
Incuber 60 min à température ambiante (à l’abri de la lumière, permet de stabiliser la couleur). -> METTRE DE LALU AVANT DE DECLENCHER LA REACTION
-
Transférer dans une cuve pour mesure de l’absorbance.
-
Mesurer l’absorbance des mixtures réactionnelles contre le blanc (voir note ci-dessous) à 420 nm au spectrophotomètre.
Blanc réactif (référence) : préparer un tube contenant le solvant et le réactif selon la même proportion (0,6 mL solvant + 0,6 mL AlCl₃ 2 %) et l’utiliser pour la correction spectrale.
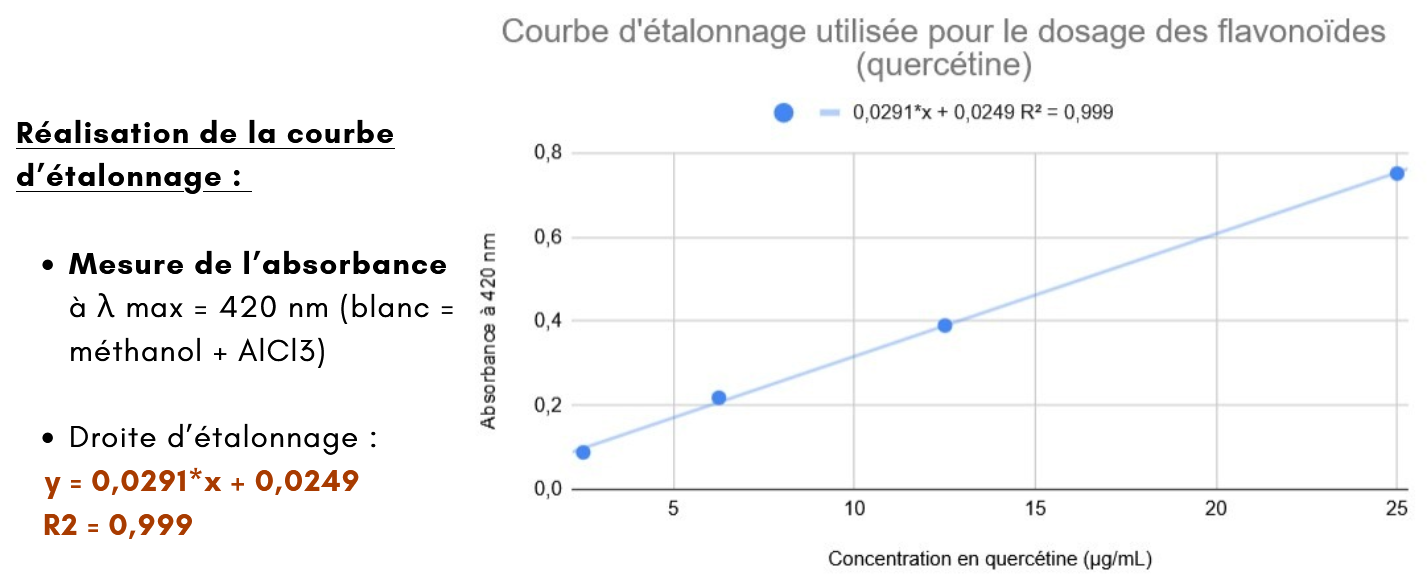
Courbe d’étalonnage & équation
-
On obtient une droite d’étalonnage pour la quercétine comme celle ci-dessous (de l’article) dans lequel on isole x afin de trouver la concentration en flavonoïdes Y = ɑ X + β
-
Y = absorbance mesurée à 420 nm
-
X = concentration en quercétine (µg/mL)
Calcul de la teneur en flavonoïdes (exprimée en mg QE / mg matière végétale sèche)
Le résultat final est exprimé en mg d’équivalent quercétine (QE) / g de matière végétale sèche. Voici la façon standard d’effectuer la conversion à partir des données acquises (variables à remplacer selon nos valeurs mesurées) :
-
Soit C = concentration calculée à partir de la droite d’étalonnage (µg/mL) — concentration dans la solution analysée (celle obtenue après dissolution de 10–50 mg d’extrait dans 5 mL).
-
Soit V_analyse = volume total de la solution d’extrait (mL) — ici 5,0 mL
-
Soit m_végétal = masse de matière sèche végétale utilisée pour l’extraction (g) — ex. 10 g
La teneur totale en flavonoïdes est exprimée comme ceci :
Références bibliographiques
Babu, A. K., Kumaresan, G., Antony Aroul Raj, V., & Velraj, R. (2018). Review of leaf drying: Mechanism and influencing parameters, drying methods, nutrient preservation, and mathematical models. Renewable and Sustainable Energy Reviews, 90, 536–556. https://doi.org/10.1016/j.rser.2018.04.002
Biesaga, M. (2011). Influence of extraction methods on stability of flavonoids. Journal of Chromatography A, 1218(18), 2505–2512. https://doi.org/10.1016/j.chroma.2011.02.059
Chandra, S., Khan, S., Avula, B., Lata, H., Yang, M. H., ElSohly, M. A., & Khan, I. A. (2014). Assessment of total phenolic and flavonoid content, antioxidant properties, and yield of aeroponically and conventionally grown leafy vegetables and fruit crops: A comparative study. Evidence-Based Complementary and Alternative Medicine, 2014, 253875. https://doi.org/10.1155/2014/253875
Chaves, J. O., de Souza, M. C., da Silva, L. C., Lachos-Perez, D., Torres-Mayanga, P. C., Machado, A. P. F., Forster-Carneiro, T., Vázquez-Espinosa, M., Velasco González-de-Peredo, A., Fernández Barbero, G., & Rostagno, M. A. (2020). Extraction of flavonoids from natural sources using modern techniques. Frontiers in Chemistry, 8, 507887. https://doi.org/10.3389/fchem.2020.507887
Résultats obtenus :
Dosages réalisés avec la pince multipigment :
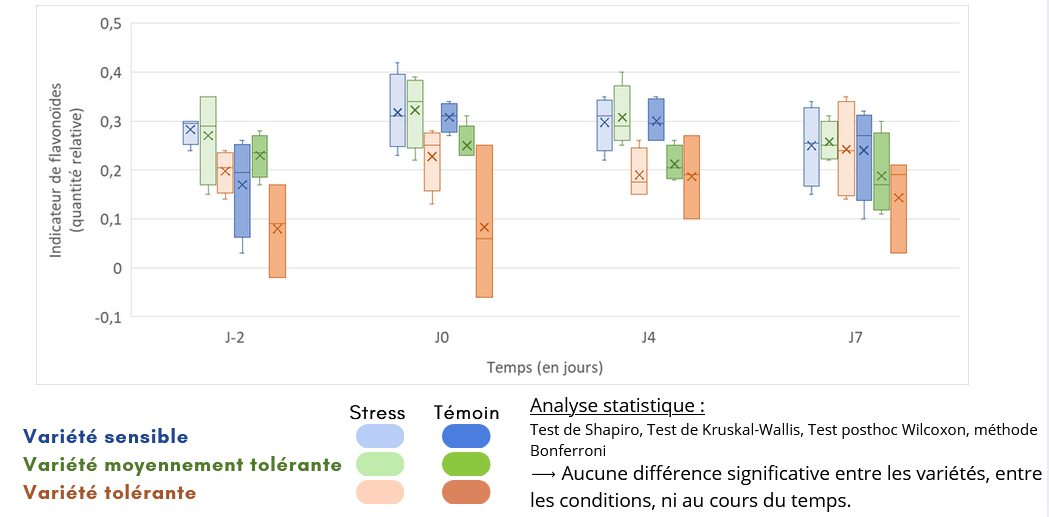
Fig.1 : Evolution de la quantité de flavonoïdes dans les plantules au cours du temps
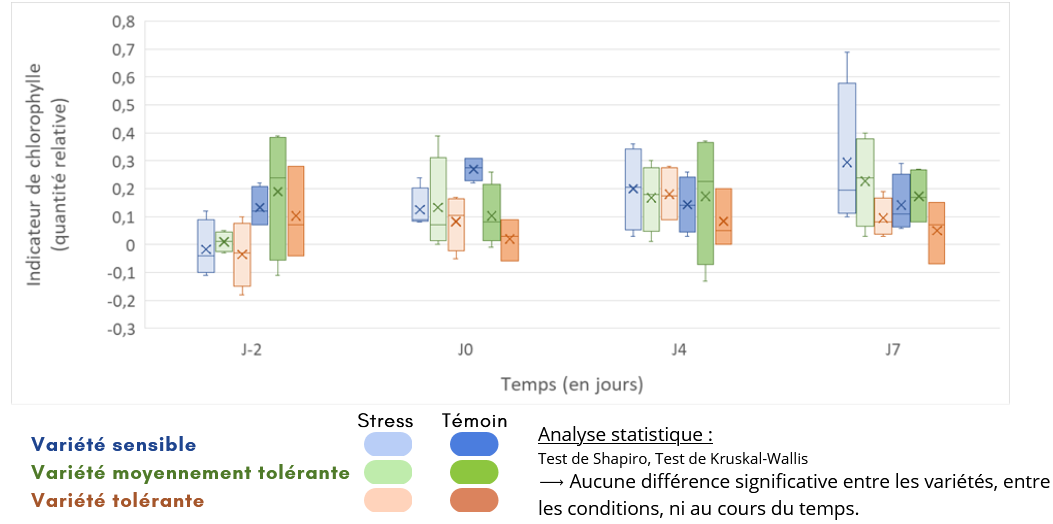
Fig. 2 : Evolution de la quantité de chlorophylle dans les plantules au cours du temps
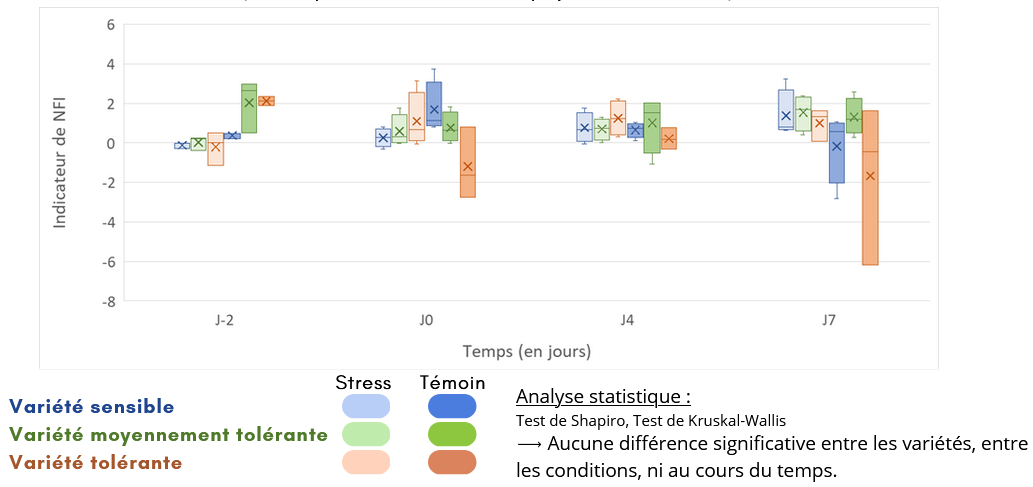
Fig. 3 : Evolution de la NFI (indice de statut azoté) dans les plantules au cours du temps (correspondant au ratio chlorophylle/flavonoïdes)
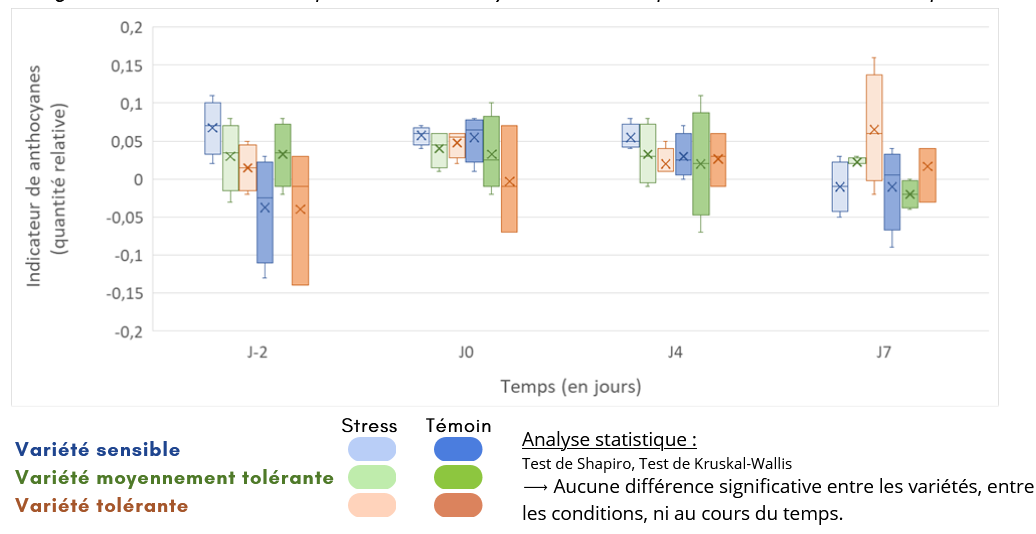
Fig. 4 : Evolution de la quantité d’anthocyanes dans les plantules au cours du temps
Dosage colorimétrique
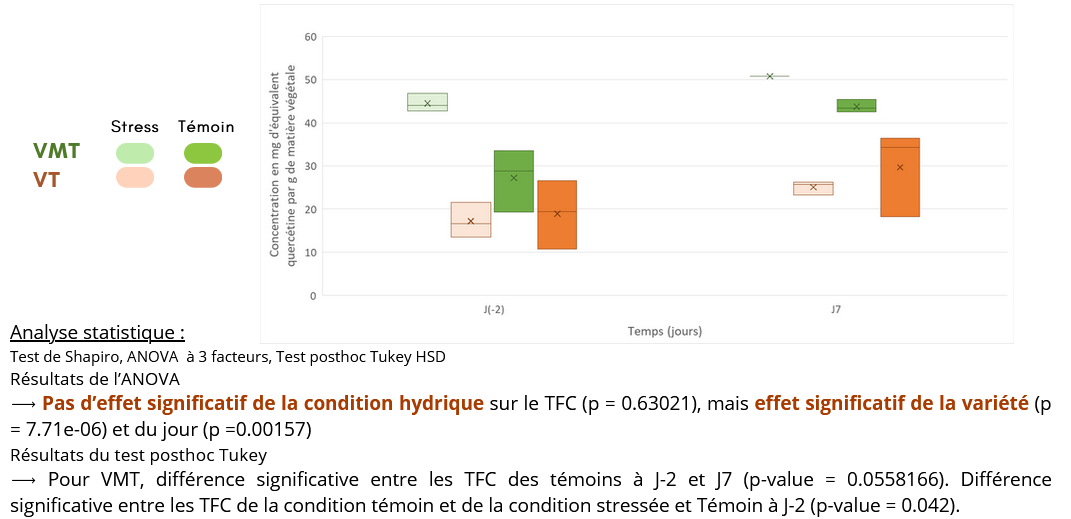
Fig. 5 : Evolution de la concentration en flavonoïdes (équivalent de quercétine) dans la matière végétale







No Comments